gull
| eiendommer | ||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
|
[ Xe ] 4 f 14 5 d 10 6 s 1
79 Au
Periodiske tabell
|
||||||||||||||||||||||||||||||||||||||||
| Som regel | ||||||||||||||||||||||||||||||||||||||||
| Navn , symbol , atomnummer | Gull, Au, 79 | |||||||||||||||||||||||||||||||||||||||
| Elementkategori | Overgangsmetaller | |||||||||||||||||||||||||||||||||||||||
| Gruppe , periode , blokk | 11 , 6 , d | |||||||||||||||||||||||||||||||||||||||
| Utseende | metallisk gul | |||||||||||||||||||||||||||||||||||||||
| CAS -nummer |
7440-57-5 |
|||||||||||||||||||||||||||||||||||||||
| EF -nummer | 231-165-9 | |||||||||||||||||||||||||||||||||||||||
| ECHA InfoCard | 100.028.332 | |||||||||||||||||||||||||||||||||||||||
| ATC -kode |
V10 AX06 |
|||||||||||||||||||||||||||||||||||||||
| Massefraksjon av jordens konvolutt | 0,004 spm [1] | |||||||||||||||||||||||||||||||||||||||
| Atomisk [2] | ||||||||||||||||||||||||||||||||||||||||
| Atommasse | 196,966570 (4) [3] et al | |||||||||||||||||||||||||||||||||||||||
| Atomradius (beregnet) | 135 (174) pm | |||||||||||||||||||||||||||||||||||||||
| Kovalent radius | 136 pm | |||||||||||||||||||||||||||||||||||||||
| Van der Waals radius | 166 pm | |||||||||||||||||||||||||||||||||||||||
| Elektronkonfigurasjon | [ Xe ] 4 f 14 5 d 10 6 s 1 | |||||||||||||||||||||||||||||||||||||||
| 1. Ioniseringsenergi | 9 . 225 554 (4) eV [4] ≈ 890 . 13 kJ / mol [5] | |||||||||||||||||||||||||||||||||||||||
| 2. Ioniseringsenergi | 20. 203 (25) eV [4] ≈ 1 949. 3 kJ / mol [5] | |||||||||||||||||||||||||||||||||||||||
| 3. Ioniseringsenergi | 30. 0 (1.6) eV [4] ≈ 2890 kJ / mol [5] | |||||||||||||||||||||||||||||||||||||||
| 4. Ioniseringsenergi | 45 . 0 (1.7) eV [4] ≈ 4340 kJ / mol [5] | |||||||||||||||||||||||||||||||||||||||
| 5. Ioniseringsenergi | 60 0 (1.9) eV [4] ≈ 5 790 kJ / mol [5] | |||||||||||||||||||||||||||||||||||||||
| Fysisk [2] | ||||||||||||||||||||||||||||||||||||||||
| Fysisk tilstand | fikset | |||||||||||||||||||||||||||||||||||||||
| Krystallstruktur | Kubisk områdesentrert | |||||||||||||||||||||||||||||||||||||||
| tetthet |
målt: 19,32 g / cm³ (20 ° C ); [6] beregnet: 19,302 g / cm³ [7] |
|||||||||||||||||||||||||||||||||||||||
| Mohs hardhet | 2,5 til 3 | |||||||||||||||||||||||||||||||||||||||
| magnetisme | diamagnetisk ( Χ m = -3,5 · 10 −5 ) [8] | |||||||||||||||||||||||||||||||||||||||
| Smeltepunkt | 1337,33 K (1064,18 ° C) | |||||||||||||||||||||||||||||||||||||||
| kokepunkt | 3243 K [9] (2970 ° C) | |||||||||||||||||||||||||||||||||||||||
| Molar volum | 10,21 · 10 −6 m 3 · mol −1 | |||||||||||||||||||||||||||||||||||||||
| Fordampningsvarme | 342 kJ / mol [9] | |||||||||||||||||||||||||||||||||||||||
| Fusjonsvarme | 12,55 kJ mol −1 | |||||||||||||||||||||||||||||||||||||||
| Lydens hastighet | 2030 m s −1 | |||||||||||||||||||||||||||||||||||||||
| Spesifikk varmekapasitet | 128 J kg −1 K −1 | |||||||||||||||||||||||||||||||||||||||
| Arbeidsfunksjon | 5.1 eV [10] | |||||||||||||||||||||||||||||||||||||||
| Elektrisk ledningsevne | 45,5 · 10 6 A · V −1 · m −1 | |||||||||||||||||||||||||||||||||||||||
| Termisk ledningsevne | 320 W m −1 K −1 | |||||||||||||||||||||||||||||||||||||||
| Kjemisk [2] | ||||||||||||||||||||||||||||||||||||||||
| Oksidasjonstilstander | −1, 0, +1, +2, +3 , +5 | |||||||||||||||||||||||||||||||||||||||
| Normalt potensial | 1,52 V (Au 3+ + 3 e - → Au) | |||||||||||||||||||||||||||||||||||||||
| Elektronegativitet | 2,54 ( Pauling -skala ) | |||||||||||||||||||||||||||||||||||||||
| Isotoper | ||||||||||||||||||||||||||||||||||||||||
|
||||||||||||||||||||||||||||||||||||||||
| For andre isotoper, se liste over isotoper | ||||||||||||||||||||||||||||||||||||||||
| NMR -egenskaper | ||||||||||||||||||||||||||||||||||||||||
|
||||||||||||||||||||||||||||||||||||||||
| sikkerhetsinstruksjoner | ||||||||||||||||||||||||||||||||||||||||
|
||||||||||||||||||||||||||||||||||||||||
| Så langt som mulig og vanlig brukes SI -enheter . Med mindre annet er angitt, gjelder dataene som gis for standardbetingelser . |
||||||||||||||||||||||||||||||||||||||||
Gull (middels høyt tysk Golt; allerede althochdeutsch gull, til indoeuropeisk rot * g h el-, gul ' [12] ) er et kjemisk element med elementets symbol Au ( latinsk aurum) og atomnummer 79. Det er en overgang metall og er i det periodiske systemet i den første undergruppen (gruppe 11), som også er kjent som kobbergruppen . Denne gruppen inneholder kobber og edle metaller sølv og gull. De tre metallene blir også referert til som "myntmetaller" i kjemi. Videre inneholder gruppen også den kunstig produserte, radioaktive og ekstremt kortvarige Roentgenium , som så langt ikke har hatt noen applikasjoner. Gull har blitt brukt til rituelle gjenstander og smykker i årtusener så vel som siden det 6. århundre f.Kr. I form av gullmynter brukt som betalingsmiddel. Gullgruvedrift, en forutsetning for utviklingen innen håndverk og metallbearbeiding, men også en faktor i gjensidig utslettelse av folk, blir kritisert over hele verden på grunn av den betydelige miljøpåvirkningen.
historie
I tidligere tider ble gull funnet i naturen som et solid metall på grunn av sin slående skinnende gule farge. Den kan bearbeides veldig godt og tærer ikke. På grunn av utholdenheten i glansen, sjeldenheten, den tilsynelatende udødeligheten og den merkbare tyngden , ble den brukt i mange kulturer først og fremst til fremtredende rituelle gjenstander og smykker.
Forhistorie og tidlig historie
Gull er et av de første metallene som ble behandlet av mennesker. Gullgruvedrift har blitt bevist siden tidlig kobberalder . Den lette legeringen med mange metaller, den moderate smeltetemperaturen og de gunstige egenskapene til legeringene gjorde gull veldig attraktivt som materiale.
Den eldste kjente gull gjenstander av menneskeheten er i alt ca. 3000 gull gjenstander fra den grav Varna (Bulgaria), som ble deponert som gravgodset og ble gjort mellom 4600 og 4300 BC. Skal dateres. [13] Mer enn 7000 gullgjenstander er fra det fjerde årtusen f.Kr. Kjent fra graver fra den østeuropeiske Maikop -kulturen . [14] Det tidligste beviset i Sentral -Europa er de to gullskivene i depotfunnet i Stollhof ( Nedre Østerrike ) og stammer også fra det fjerde årtusen f.Kr. Siden den gang har gull blitt importert fra Sørøst -Europa i form av smykker.
I Sentral- og Nord -Europa dukket det ikke opp gyldne gjenstander før det tredje årtusen f.Kr. BC som gravgods, spesielt i sen neolittisk klokkebegerkulturen . Eksempler er øredobber og hårklips ved bueskytteren i Amesbury eller gullringene som ble funnet i 2013 i en klokkeformet grav fra Wustermark , Havelland-distriktet . [15] [16] Berømte eksempler fra den følgende bronsealderen er gullputene Nebra sky disk ( tidlig bronse ) og de fire sene bronse gullhatter .
De gamle egypterne utnyttet forekomster i Øvre Egypt og Nubia . [17] Papyrus i Torino viser også plasseringen av en gullgruve. Romerne brukte steder i Lilleasia , Spania ( Las Médulas ), Romania og Germania .
Legenden om reisen til Argonautene til Golden Fleece i Colchis var tilsynelatende inspirert av sjøreisene til greske prospektører.
Toraen forteller om gullkalven , som israelittene laget som et avgud mens Moses mottok de ti bud , og om det gylne landet Ofir . Det nye testamente nevner gull (sammen med røkelse og myrra ) som en av hyllestgavene fra de vise mennene i Orienten til den nyfødte Jesus ( Matt 2:11 EU ).
Gull ble behandlet veldig tidlig i Sør -Amerika og Mesoamerika . For eksempel mestret Mochica i Peru allerede dannelsen av legeringer ( tumbago ) og forgylling i begynnelsen av det første årtusen og laget gjenstander for rituelle formål fra flere kilo gull.
Gull ble ekstrahert og renset ved panorering for gull , sammensmeltning og kupellering (oksiderende basismetaller med bly , også kalt raffinering ) eller en kombinasjon av disse prosessene.
Middelalder og moderne tid
Sent middelalderske og tidlige moderne forfattere, spesielt innen alkymi , antok at gull ble skapt ved å blande "rent" svovel og kvikksølv. I medisin ble polert gull blant annet brukt som medisin mot epilepsi. [18]
Med de europeiske maritime maktenes overherredømme Spania, Portugal, England og Italia, ble grådigheten for gull en avgjørende årsak til kriger og erobringer i moderne tid . Spesielt gullrikdommen til urfolket i Sentral- og Sør -Amerika tiltrukket europeiske og spesielt spanske erobrere ( conquistadores ) etter oppdagelsen av Amerika i 1492, som brakte gull til Europa i galleoner . For en tid ble Spania den rikeste nasjonen i Europa; urfolkskulturen ble ødelagt av erobrerne eller av sykdommer som ble ført inn.
Gang på gang tiltrukket gullfunn et stort antall eventyrere. På 1800 -tallet var det massebevegelser av gullsøkere til områdene med store gullforekomster på forskjellige kontinenter, kjent som gullrushet . Eksempler er gullrushet i California i 1849 og gullrushet fra 1897 på Klondike -elven i Alaska . Det var også et gullrushet i Australia ( Bathurst , Temora , Teetulpa og Coolgardie ) og Sør -Afrika ( Witwatersrand ).
Den svingende gullprisen fører ofte til betydelige sosiale endringer: For eksempel førte en fallende gullpris i Sør -Afrika til en alvorlig forringelse av den delen av befolkningen som lever på gullgruvedrift. I den brasilianske Amazonas er den uformelle gullgruvedriften av Garimpeiros ofte forbundet med alvorlige sosiale og økologiske konsekvenser.
Skje
Gullinnholdet i den kontinentale skorpen er 4 ppb , [1] omtrent 4 gram per 1000 tonn stein. Andelen svinger avhengig av region - i forekomster som blir utvunnet, er gullandelen ofte flere gram per tonn.
Gull forekommer hovedsakelig i fast form på jorden, dvs. i elementær, metallisk form. Det er funnet i primærråstoff innskudd som gull inneholdende sten ( gullmalm ) og i sekundær innskudd i, blant annet, såpe avleiringer .
Omtrent 43% av gullet som ble utvunnet i 2017 kom fra Folkerepublikken Kina , Australia , USA , Russland og Canada . [19] De dypeste gullgruvene i verden er i Sør -Afrika. Det er gull utvunnet nesten 4000 meter under jordoverflaten. I begynnelsen av 2011 planla gruveselskapet AngloGold Ashanti allerede sjakter på opptil 5000 meters dyp. [20]
I 2016 var rundt 17% av gullmengdene som ble ekstrahert et biprodukt fra raffinering av andre metaller som kobber , nikkel eller andre edle metaller , [21] slik at utvinning av gull som et biprodukt kan gjøre utnyttelsen av andre innskudd økonomiske.
Totalt har nesten 2700 nettsteder for solid gull blitt dokumentert over hele verden så langt (fra 2017). [22]
Opprinnelsen til det jordiske gullet
De fleste elementene ned til jern, men tyngre enn hydrogen, ble dannet i tidligere stjerner med frigjøring av energi gjennom kjernefusjoner (se også nukleosyntese ). Gullet som forekommer på jorden - som alle andre grunnstoffer som er tyngre enn jern - ble skapt av supernova -kjernekollaps mens den absorberte energi.
Datasimuleringer utført i 1994 spådde at når to nøytronstjerner kolliderer, ville materialet som kastes ut i verdensrommet og de påfølgende reaksjonskaskadene produsere rundt 30 masser av gull i tillegg til andre tunge elementer. 17. august 2017 registrerte LIGO -detektorene gravitasjonsbølger som ble tolket som en kollisjon mellom to nøytronstjerner i en avstand på 130 millioner lysår. Reaksjonene til det utkastede stoffet kunne deretter observeres med optiske teleskoper. De målte spektrallinjene bekreftet spådommen om at store mengder gull og andre tunge elementer ble dannet under denne hendelsen. [23]
Så lenge den tidlige jorden ikke hadde en solid skorpe, vandret alt gull inn i jordens indre på grunn av dens høye tetthet. Vi finner bare gull som nådde jorden etter skorpedannelse eller som kom tilbake til overflaten gjennom vulkanske prosesser.
Primære forekomster (fjellgull)
Følgende seksjoner viser noen av hovedtypene primære gullforekomster :
Witwatersrand type (innskudd i paleo-såpe)
Witwatersrand gullfelt i Sør -Afrika er det desidert største i verden. Til dags dato har dette innskuddet levert mer enn 52 000 tonn gull. [24] Den malmkropper er frühproterozoische (omtrent 1,8 milliarder år gammel) paleo -Flussschotter at nativt gull, pyritt og lokalt minable konsentrasjoner av bekblende inneholde (uranmalm). Den eksakte opprinnelsen til innskuddet var kontroversiell i lang tid. Depositumet er nå tolket som et rent paleosåpe- forekomst , noe som betyr at det faller inn under de sekundære avsetningene. Omtrent 25% av gullet som er funnet, har en form som er typisk for transport gjennom hydrotermiske løsninger, mens 75% av gullet er de typiske nuggets som snakker om fluvial transport, som i dag omtales som påfølgende mobilisering av Running out of gold. [25] Nyere isotopundersøkelser tyder på at en veldig liten hydrotermisk mobilisering av gullet på noen få millimeter til centimeter fant sted, slik at dette gullet sannsynligvis opprinnelig kom fra elvegruset. [26] Tilstedeværelsen av avrundede pyritt- og pitchblende -klaster viser uansett at disse tilhørte den opprinnelige bestanden av elvegrus. De indikerer dermed at jordens atmosfære på dette tidspunktet bare kunne ha hatt et lavt oksygeninnhold, siden disse mineralene ikke er stabile under oksiderende forhold.
Ressursene til innskuddet er fremdeles titusenvis av tonn gull, om enn på en betydelig dybde. Her er de dypeste gruvene i verden (nesten 4000 m); gruvedrift er derfor bare økonomisk når gullprisene er høye. Depositumet står for 40% av gull pluss ressurser som er utvunnet over hele verden til dags dato. [27]
Orogenholdige gullforekomster
Noen av de viktigste gullforekomstene på jorden tilhører de orogene (mesotermiske) veneavsetningene . Disse forekomstene forekommer hovedsakelig i metamorfe og deformerte marine sedimenter og vulkanske bergarter . De oppstår under fjelldannelse og er derfor knyttet til gamle og unge foldbelter. Under fjelldannelse frigjøres metamorfe væsker fra de involverte bergartene, som legger kvarts, en liten mengde sulfider og gull i sprekker . Væskene har en nøytral karakter og temperaturer mellom 250 ° C og 400 ° C. Sulfidene er for det meste pyritt og arsenopyritt . Gullkarakterene er vanligvis veldig høye, mer enn 10 g / t er ikke uvanlig. Forekomstene av denne typen ble dannet gjennom jordens historie med betydelige forekomster i de arkaiske grønnsteinsbelter i Afrika og Vest -Australia, under proterozoikum (USA, Ghana, Brasil), de paleozoiske forekomstene i Victoria (Australia) eller den unge alpinen forekomster i Alpene (“Tauern -Gold”).
Dette er stort sett rene gullforekomster uten mulighet for utvinning av andre metaller. Noen få forekomster inneholder imidlertid så høye nivåer av arsen at de er blant de viktigste forekomstene av dette halvmetallet .
Epitermiske gullforekomster
Epitermiske gullforekomster er nært knyttet til ung bergmagmatisme ved subduksjonssoner ( øybuer , kollisjoner mellom hav og kontinent). Varme hydrotermiske væsker fra magma eller hydrotermiske væsker oppvarmet av magmatismen transporterer gullet og deponerer det i tunneler , i form av lagermineralisering eller som impregnering i fjellet. Det skilles mellom “lavsulfidering” og “høysulfidering” -epi termiske forekomster, som er preget av forskjellige væsker og tilhørende forskjellige mineralinnhold. [28] "Lavsulfiderende" forekomster dannes fra nøytralt hydrotermisk vann med temperaturer på 200 til 300 ° C, mens avsetninger med "høy sulfidasjon" dannes av svært sure og oksiderende væsker med opptil 300 ° C. Begge typene er forskjellige når det gjelder mineralveiledning. Malmkvaliteter er vanligvis mellom 1 og 10 g gull per tonn og et gullinnhold på noen få til over 1000 tonn. Noen forekomster med høy sulfidasjon inneholder store mengder sølv og ikke-jernholdige metaller . Nyere studier fra aktive hydrotermiske felt i New Zealand indikerer at store forekomster av denne typen med 1000 t gullinnhold kan dannes på bare 50 000 år.
Det er betydelige eksempler på denne typen innskudd i blant annet Papua Ny -Guinea , New Zealand , Mexico , Peru og Romania.
Type Carlin
Denne typen består av forekomster i karbonatbergarter . De viktigste forekomstene av denne typen er i Utah og Nevada ( USA ). Forekomstene der dannet seg i et kort intervall mellom 42 og 30 millioner år siden. De ble dannet av reduserte, moderat sure væsker med temperaturer på 150 til 250 ° C på dybder over 2000 m. Malmlegemene kan inneholde noen få til mer enn 100 millioner tonn malm med grader mellom 1 og 10 g / t. Gull er stort sett bundet til findelt arsenrik pyritt . Som et resultat er behandlingen av disse malmene relativt kompleks.
IOCG (jernoksid-kobber-gull) type
IOCG -forekomster forekommer i bergartede vulkanske bergarter som granitter og rhyolitter . Dette er store hydrotermiske breccia -kropper med høye nivåer av jern i form av hematitt og / eller magnetitt . Disse avsetningene ble sannsynligvis dannet under et vulkansk kompleks. Under et utbrudd førte hydrotermiske væsker til dannelse av breccia fra vulkanske bergarter og avsatte jernoksider, kobbersulfider, innfødt gull og andre mineraler. De viktigste forekomstene av denne typen er i meso proterozoiske bergarter i Australia som Earnest Henry ( Queensland ), Prominent Hill og Olympic Dam (begge i delstaten Sør -Australia ). Sistnevnte representerer et av de største malmlegemene på jorden med for tiden antatte ressurser på 8,4 milliarder tonn malm. Malmkvaliteten er mellom 0,5 og 2% for kobber og 0,5 og 1,5 g / t for gull. De fleste forekomster av denne typen inneholder rent kobber og gull, mens Olympic Dam også inneholder uran og sølv. Dette forekomsten representerer den største kjente uranforekomsten på jorden.
Porphyry Cu-Au avsetninger
Slike forekomster finnes over hele verden i unge fjellkomplekser. De er store malmlegemer i mellomliggende til sure plutoniske vulkanske bergarter. De malmmineraler (svovelkis, kobberkis , bornitt , chalcosine , molybdenitt ) forekommer fint fordelt over et nettverk av sprekker i fjellet. Malmkroppene inneholder titalls millioner til flere milliarder tonn malm. Den største forekomsten av denne typen er Chuquicamata i Chile med over 10 milliarder tonn malm. I USA er Bingham Canyon det viktigste forekomsten og en av de største gullprodusentene i landet. Malmkvaliteten er relativt lav med 0,5 til 1% kobber og 0,1 til 1 g / t gull, men størrelsen på malmlegemene tillater økonomisk utvinning. Ofte er disse avsetningene assosiert med skarnforekomster, og det er epitermiske gullforekomster i det større området.
VHMS / SHMS innskudd
Disse forekomstene dannes i havområdet. Volcanic Hosted Massive Sulphides (VHMS) er bundet til grunnleggende vulkanske bergarter (for det meste basalter ), mens Sediment Hosted Massive Sulphides (SHMS) forekommer i marine sedimentære bergarter. Meist handelt es sich bei diesen Lagerstätten um reine Buntmetalllagerstätten ( Blei , Zink , Kupfer ), einige enthalten aber auch gewinnbare Beimengungen von Gold, Silber und anderen Elementen. Die devonische SHMS-Lagerstätte Rammelsberg bei Goslar im Harz stellt mit 28 Millionen Tonnen Erz und einem Goldgehalt von 1 g/t als Beimengung zu den extrem hohen Blei- und Zinkgehalten die bedeutendste deutsche Goldlagerstätte dar.
Sekundäre Lagerstätte (Waschgold/Seifengold)
Fast alle europäischen Flüsse führen Spuren von Gold mit sich. Dieses Gold war zuvor in Form zumeist kleiner, dünner Blättchen in Gestein eingelagert. Durch Verwitterungsprozesse des umgebenden Gesteins wird es freigesetzt und gelangt so ins Flusswasser und wird als Fluss-Seife abgelagert.
Auf den Geröllbänken des Hoch- und Oberrheines wie bei Istein finden sich davon geringe Mengen, insbesondere Flitter . Diese, als Rheingold bezeichneten Sekundärablagerungen, wurden in den vergangenen Jahrhunderten mit mäßigem Ertrag ausgewaschen (siehe dazu Flussgolddukaten ). Der einzige offizielle Goldproduzent Deutschlands, ein seit 2008 zur Holcim -Gruppe [29] gehörendes Kieswerk bei Rheinzabern , nutzt ebenfalls diese Vorkommen. [30]
Förderung weltweit
Die Weltjahresförderung betrug 2008 noch 2.260 Tonnen, 2011 bereits 2.700 Tonnen, etwa hundertmal mehr als im 19. Jahrhundert. Aktuell wird in zwei Jahren mehr Gold gefördert, als in den tausend Jahren des Mittelalters zusammen dokumentiert ist.
Das meiste Gold wurde lange Zeit in Südafrika gefördert, dessen Fördermengen jedoch bereits seit den 1970er Jahren sinken. Im Jahr 2007 förderte Australien die größte Menge. Seit 2008 stammt die größte Fördermenge aus der Volksrepublik China , gefolgt von Australien. Ebenfalls seit 2008 fördern die USA mehr Gold als Südafrika, seit 2010 liegt die Fördermenge der Russischen Föderation über der von Südafrika. [31]
| Rang 2011 |
Land | Fördermenge (in t) | Reserven 2014 7 |
Reichweite (Jahre ab 2014) 7 |
||
|---|---|---|---|---|---|---|
| 2007 1 | 2011 4 | 2014 7 | ||||
| 1 |
|
275 | 355 | 450 | 3.000 | 6,7 |
| 2 |
|
246 | 270 | 270 | 9.800 | 36,3 |
| 3 |
|
157 | 200 | 245 | 5.000 | 20,4 |
| 4 |
|
238 | 237 | 211 | 3.000 | 14,2 |
| 5 |
|
101 | 110 | 160 | 2.000 | 12,5 |
| 6 |
|
252 | 190 | 150 | 6.000 | 40 |
| 7 |
|
170 | 150 | 150 | 2.100 | 14 |
| 8 |
|
85 | 90 | 102 | 1.700 | 16,7 |
| 9 |
|
39 | 85 | 92 | 1.400 | 15,2 |
| 10 |
|
84 | 100 | 90 | 2.000 | 22,2 |
| 11 |
|
40 | 55 | 70 | 2.400 | 34,3 |
| 12 |
|
118 | 100 | 65 | 3.000 | 46,2 |
| 13 |
|
65 | 70 | 60 | 1.200 | 20 |
| 14 |
|
42 | 45 | 50 | 3.900 | 78 |
|
|
471 | 630 | 695 | 10.000 | 14,4 | |
| Summe (gerundet) | 2.380 | 2.700 | 2.860 | 55.000 | 19,2 | |
Weltweit existieren nur einige große Goldförderunternehmen, deren Aktien an den Börsen gehandelt werden. Dazu gehören etwa Agnico Eagle Mines , AngloGold Ashanti , Barrick Gold , Freeport-McMoRan Copper & Gold, Gold Fields Ltd. , Goldcorp , Kinross Gold , Newmont Mining und Yamana Gold .
Goldbestand weltweit
In der gesamten Geschichte der Menschheit wurden bis Ende 2017 schätzungsweise 190.000 Tonnen gefördert. [32] Dies entspricht einem Würfel mit 21 Metern Kantenlänge [33] (rund 8800 Kubikmetern) reinem Gold, und rund 24,3 g (also etwas mehr als ein Kubikzentimeter) pro Kopf der Weltbevölkerung. Etwa 34.000 Tonnen (Stand 2019) befinden sich im Besitz von Zentralbanken, siehe auch Goldreserve .
Vorkommen in Europa
Die Förderung von Gold in Europa – am meisten in Finnland und Schweden – ist im internationalen Vergleich unbedeutend. Die rumänischen Golderzvorkommen sind wohl die größten in Europa. In Bulgarien finden in den stillgelegten Goldminen Zlata (aktiver Bergbau: 1939–1973) und Krushov Dol (aktiv: 1965–1974) wieder Erkundungen statt. [34] In Barsele (in der Gemeinde Storuman ) in Schweden wurde ein Vorkommen erkundet. [35]
Gold als Mineral
Natürliche Vorkommen an gediegen Gold, das heißt in seiner elementaren Form waren bereits lange vor der Gründung der International Mineralogical Association (IMA) bekannt. Gold ist daher als sogenanntes grandfathered Mineral als eigenständige Mineralart anerkannt. [36]
Gemäß der Systematik der Minerale nach Strunz (9. Auflage) wird Gold unter der System-Nr. „1.AA.05“ (Elemente – Metalle und intermetallische Verbindungen – Kupfer-Cupalit-Familie – Kupfergruppe) [37] beziehungsweise in der veralteten 8. Auflage unter I/A.01 (Kupfer-Reihe) eingeordnet. Die vorwiegend im englischsprachigen Raum verwendete Systematik der Minerale nach Dana führt das Element-Mineral unter der System-Nr. „01.01.01.01“ (Goldgruppe). [38]
In der Natur findet sich Gold üblicherweise in Form von abgerundeten Nuggets, als Schuppen oder Flocken sowie in dendritischen (baumartigen) oder haar- bis drahtförmigen Aggregaten . Selten entwickelt Gold grobkristalline Stufen mit oktaedrischen , dodekaedrischen und würfeligen Kristallen. Es kann mit verschiedenen Mineralen vergesellschaftet sein wie unter anderem Altait , Ankerit , Arsenopyrit , Calaverit , Chalkopyrit , Krennerit , Pyrit , Pyrrhotin , Quarz , Scheelit , Sylvanit (Schrifterz) , Tetradymit und Turmalin . [7]
Da Gold ein reaktionsträges Element ist, behält es gewöhnlich seinen Glanz und Farbe und ist daher in der Natur leicht zu erkennen. Dennoch wird es immer wieder mit farblich ähnlichen Mineralen wie Pyrit ( Katzengold , Narrengold ) und Chalkopyrit verwechselt. Gold ist zudem ein Bestandteil verschiedener Mineralarten. Beispiele für Minerale mit den höchsten Goldgehalten sind unter anderem Bezsmertnovit ((Au,Ag) 4 Cu(Te,Pb); 78,56 % Au), Tetra-Auricuprid (CuAu; 75,61 % Au), Maldonit (Au 2 Bi; 65,34 % Au) und Yuanjiangit (AuSn; 62,40 % Au). Insgesamt sind bisher 33 Gold-Minerale bekannt (Stand 2017). [39]
Gewinnung
Im Gegensatz zu den meisten anderen Metallen kommt das chemisch inerte Gold meist gediegen vor und muss nicht durch Reduktion aus Erzen gewonnen werden, wie beispielsweise Eisen . Es wird zunächst nur mechanisch aus dem umgebenden Gestein gelöst. Da Gold chemisch wenig reaktiv ist und somit nur schwierig in lösliche Verbindungen überführt werden kann, werden spezielle Verfahren zur Goldgewinnung angewendet.
Ohne Lupe direkt sichtbares Gold, sogenanntes „Freigold“ [40] in Form von Nuggets oder Goldstaub, ist eine Rarität. Das größte bekannte Goldnugget wurde im September 2018 von Henry Dole in Australien gefunden, mit rund 2400 Unzen (74 kg) Goldanteil. [41] Der zweitgrößte Goldnugget, „Welcome Stranger“ genannt, wurde 1869 in Australien gefunden und wog 2284 Feinunzen [42] (rund 71 kg). Das meiste Gold in den Vorkommen liegt in kleinsten Partikelchen im umgebenden Gestein fein verteilt vor und entgeht somit den Versuchen, es mit einfachen Verfahren manuell zu sammeln.
In der Praxis werden mehrere Verfahren miteinander kombiniert, um die gewünschte hohe Ausbeute zu erhalten. Durch Fortschritte in den Gewinnungsmethoden, Vernachlässigung der Abfallproblematik und bei hohem Marktpreis lohnt sich sogar der Abbau von Erz, das nur ein Gramm Gold pro Tonne enthält. Alte Abraumhalden ehemaliger Goldvorkommen werden deshalb mittels verbesserter Technik nochmals aufgearbeitet.
Gold fällt als Nebenprodukt bei der Raffination anderer Metalle an und wird in großem Umfang wiedergewonnen. Mehr als zehn Prozent des weltweit abgebauten Goldes wird im Kleinbergbau gewonnen. Es wurde geschätzt, dass 20 % bis 30 % des weltweit geförderten Goldes durch nicht industrielles Schürfen, also von Goldsuchern gewonnen wird. [43] Ein Teil davon kann als Konfliktrohstoff betrachtet werden, der eine negative Auswirkung auf die dort lebende Bevölkerung hat und zum sogenannten Ressourcenfluch führen kann.
Goldwaschen
Das sogenannte Goldwaschen als einfachstes Verfahren zur Goldgewinnung nutzt die hohe Dichte des Metalls. Dabei wird goldhaltiger Sand mit Wasser aufgeschlämmt. Da Gold schwerer ist als der umgebende Sand, setzt es sich schneller am Boden ab und kann abgetrennt werden. Gold aus Flussablagerungen wird so gewonnen. Hobby-Goldsucher wenden meist dieses Verfahren an. Dessen Nachteil besteht jedoch in der geringen Ausbeute bei großem Zeitaufwand des Suchenden. Der Vorteil dieser Methode ist die zuverlässige Ausbeute an groben Goldteilchen, die bei der Cyanidlaugung nicht vollständig erfasst werden. Es lässt sich verbessern durch Einbringen von Fellen in die abströmende Flüssigkeit, in dem sich kleinste Goldpartikelchen in den Fellhaaren verfangen und die Ausbeute erhöhen.
Goldwaschen wird mitunter teilmechanisiert an Land durchgeführt oder mit Schwimmbaggern mit integrierter Wäsche direkt im Fluss. Minentechnisch gewonnenes Erz wird zuvor mechanisch auf geeignete Korngrößen zerkleinert und das zermahlene Gestein in ähnlicher Weise bearbeitet.
Dieses Verfahren geht der nachfolgend beschriebenen weiteren Ausnutzung der goldführenden Sande und Schlämme voraus.
Amalgamverfahren
Beim Amalgamverfahren wird die Legierungsbildung zwischen Gold und Quecksilber zu Amalgam genutzt. Zur Goldgewinnung und -reinigung werden goldhaltige Sande und Schlämme intensiv mit Quecksilber vermischt. Das Gold, aber auch eventuell andere vorhandene gediegene Metalle wie Silber lösen sich dabei im Quecksilber. Goldamalgam hat eine silberne Farbe; je nachdem, wie viel Quecksilber im Überschuss vorliegt, ist es flüssig bis pastös teigig [44] und der Schmelzpunkt der Legierung ist geringer als der von Gold. [45] Amalgam und Quecksilber sammeln sich wegen der hohen Dichte am Gefäßgrund, das Quecksilber fließt dann ab. Durch Erhitzen des verbleibenden Amalgams (wie bei Feuervergoldung detailliert beschrieben) verdampft das Quecksilber und zurück bleibt kompaktes Rohgold.
Die entstehenden Quecksilberdämpfe stellen eine gesundheitliche Gefahr dar (siehe Quecksilbervergiftung ), wenn sie nicht durch eine geschlossene Destillationsanlage oder Absaugung und Abfilterung mit Aktivkohle aufgefangen werden. Private Goldschürfer erhitzen das Amalgam oft in offenen Blechgefäßen mithilfe von Lötlampen und sonstigen Gasbrennern. Das Quecksilber (Siedepunkt 357 °C) dampft dabei in die Umgebungsluft ab und kondensiert umgehend. Dadurch werden Böden, Flüsse und Menschen in der Umgebung mit Quecksilber belastet. Durch das Minamata-Übereinkommen sollen Alternativen zum Amalgamverfahren gefördert werden. [46]
Das Amalgamverfahren wurde bereits in der Antike angewendet.
Cyanidlaugung
Bei größeren Vorkommen, die eine industrielle Erschließung erlauben, wird seit Ende des 19. Jahrhunderts die Cyanidlaugung angewendet. Vor dem Hintergrund, dass sich Gold in sauerstoffhaltiger Natriumcyanid -Lösung (Natriumsalz der Blausäure HCN) als Komplexverbindung löst, werden die metallhaltigen Sande staubfein gemahlen, aufgeschichtet und im Rieselverfahren mit der Extraktionslösung unter freiem Luftzutritt versetzt. Die kleinsten Metallteilchen werden hierbei zuerst aufgelöst, weil sie die relativ größte Reaktionsoberfläche haben.
Das Edelmetall findet sich chemisch gebunden im hochgiftigen Sickerwasser . Nach Filtration und Ausfällung mit Zinkstaub wird es als brauner Schlamm erhalten, aus dem nach Waschen und Trocknen durch Reduktion Rohgold wird.
Hier schließt sich die Reinigung des Rohgoldes an. Raffiniert zu Feingold ist es dann standardisiert und marktreif. Die Cyanidlaugen werden in Kreislaufprozessen wiederverwendet. Dennoch entweichen Blausäure und ihre Salze (Cyanide) in die Umwelt, teilweise in größeren Mengen, etwa bei Unglücken, Fehlfunktionen der Anlage oder bei Überschwemmungen. Alle diese Stoffe sind hochgiftig, allerdings leicht zersetzbar. Im Stoffkreislauf der Natur werden sie relativ schnell oxidativ abgebaut oder durch Hydrolyse zersetzt.
Diese Art der Goldgewinnung hinterlässt enorme Abraumhalden und Stäube mit Cyanidspuren. Weitere Umweltschäden entstehen dadurch, dass Schlamm in Ländern mit geringer Umweltüberwachung unkontrolliert in Flüsse abgeleitet wird oder Schlammabsetzbecken bersten, wie im Jahr 2000 im rumänischen Baia-Mare .
Boraxverfahren
Ein umweltfreundlicheres Verfahren stellt die Gold extraktion und -reinigung mithilfe von Borax (Natriumborat) dar. [47] [48] Der Zusatz von Borax als schlackenbildendes Flussmittel beim Schmelzen von verunreinigtem Gold setzt Schmelzpunkt und Viskosität der Schmelze aus Oxiden und Silikaten der Begleitstoffe ( nicht des Goldes , wie es oft fälschlicherweise angegeben wird) herab. [49] Dadurch kann das Schmelzen mit einfacheren, kostengünstigen Brennern erfolgen (mit Zusatz von Holzkohle und extra Luftzufuhr [50] [51] unter Verwendung eines Haartrockners und eines Verlängerungsrohrs bis in die Esse [52] oder eines Blasebalgs ), wobei die Ausbeute der Extraktion erhöht wird. [53] Das Gold (oder bei Anwesenheit von Silber eine Gold-Silber-Legierung) setzt sich dabei am Boden der Schmelzpfanne ab, die Oxide schwimmen auf. Gelegentlich werden andere Flussmittel zugesetzt (beispielsweise Calciumfluorid , Natriumcarbonat , Natriumnitrat oder Mangandioxid ). [54] Würden alle Goldschürfer auf der Welt dieses Verfahren anwenden, könnte die Emission von rund 1000 Tonnen Quecksilber pro Jahr vermieden werden, das sind etwa 30 % der weltweiten Quecksilber-Emissionen. [53]
Anodenschlammverfahren
Gold wird häufig aus Anodenschlämmen gewonnen, die bei der Raffination anderer Metalle, vor allem von Kupfer, zurückbleiben. Während der Elektrolyse wird das edle Gold nicht oxidiert und nicht gelöst; es sammelt sich unter der Anode an. Neben Gold fallen dabei Silber und andere Edelmetalle an, die durch geeignete Verfahren voneinander getrennt werden.
Wiedergewinnung aus Reststoffen (Recycling)
Eine wichtige Quelle des Edelmetalls ist die Aufbereitung von Dental- und Schmuckverarbeitungsabfällen sowie von alten edelmetallhaltigen Materialien, wie selektierter Elektronikschrott und Galvanikschlämme. Die Wiederaufbereitung stellte 2016 rund 30 % des gesamten Goldangebots. [55]
In städtischem Klärschlamm ist Gold in Spuren enthalten, die von der Nutzung, der Verarbeitung und dem Verschleiß von Goldlegierungen (Abrieb von Zahnfüllungen, Schmuckkettenglieder, Verlust und so weiter) stammen. Eine Untersuchung verschiedener Proben aus Arizona ergab neben verschiedenen anderen Edelmetallen einen Gehalt von durchschnittlich 0,3 Gramm Gold pro Tonne Klärschlamm. [56] 2017 konnten in einer Schlacken sortieranlage in der Schweiz 65 Kilogramm Gold im Wert von 2,1 Millionen Franken gewonnen werden. [57]
Im September 2013 berieten Österreichs Krematorienbetreiber , wie rechtlich korrekt mit dem Gold verbrannter Verstorbener umzugehen wäre, das bislang verklumpt mit Knochenasche in der Urne den Hinterbliebenen ausgefolgt wird. [58]
Versuche zur Goldgewinnung aus dem Meer
Fritz Haber versuchte in den 1920er Jahren, Gold aus dem Meerwasser zu gewinnen, womit die deutschen Reparationen bezahlt werden sollten. [59] Es wurde damals angenommen, dass Meerwasser zwischen 3 und 10 Milligramm Gold pro Tonne enthält. Der durchschnittliche Gehalt war aber mit 4,4 Mikrogramm Gold pro Tonne Meerwasser etwa um den Faktor 1000 niedriger und für eine wirtschaftliche Verwertung deutlich zu gering. [60] [61] Durch moderne Messmethoden wurde festgestellt, dass der Atlantik und der nordöstliche Pazifik 50–150 Femtomol (fmol) Gold pro Liter Wasser beinhaltet. Das entspricht 0,010–0,030 µg/m³. Im Tiefenwasser des Mittelmeeres lassen sich eher höhere Werte von 100–150 fmol Gold pro Liter Meerwasser messen. Insgesamt ergibt das 15.000 Tonnen Gold in den Weltmeeren. [62]
Goldsynthese
Die Hoffnung, Gold künstlich herstellen zu können, wurde von vielen Kulturen über Jahrhunderte gehegt. Dabei entstand unter anderem die Sage vom sogenannten Stein der Weisen , der Gold aus unedlen Metallen entstehen lassen sollte. Die Alchemie wurde gelegentlich als „künstliche Darstellung von Silber und Gold“ oder schlicht als „Goldmacherei“ aufgefasst. [63]
Beispielsweise wird in zwei ostmitteldeutschen Handschriften des 15. Jahrhunderts ein Nikolaus von Paris genannt, nach dessen alchemistischem Traktat Von silber unde von golde Gold hergestellt werden könne, indem Silber und „rotes Eisen“ mit Salmiak versetzt werden, diese Mischung eine Woche in heißem Pferdemist belassen wird, danach gefiltert und auf die Hälfte eingedampft wird und mit der dadurch entstandenen Substanz Silber in 12-karätiges Gold transmutiert werden könne. Wenn dann ein Teil dieses Goldes mit vier Teilen natürlichem Gold gemischt wird, solle 20-karätiges Gold entstehen. [64]
Tatsächlich entsteht Gold allein bei verschiedenen kerntechnischen Prozessen ( Kernfusion beziehungsweise Kernfission ) in winzigen Mengen.
Umweltauswirkungen
Da Gold in heutigen Minen fast nur noch in Spuren enthalten ist, fallen alleine zur Produktion eines einzigen Goldrings 20 Tonnen Schutt an, was zu einer beträchtlichen Zerstörung ganzer Landschaften führt. [65] Beträchtliche Mengen von hochgiftigem Quecksilber , schon bei der Goldgewinnung mit ausgeschwemmt oder beim Verdampfen wissentlich in die Umwelt freigesetzt, vergiften zudem große Gebiete und Flussläufe dauerhaft. [66] Da Goldgewinnung oft improvisatorische Züge trägt und fernab von effektiver behördlicher Überwachung stattfindet, werden Umweltaspekte häufig untergeordnet behandelt oder ignoriert. [67]
Die negativen Umweltauswirkungen führen häufig zu Konflikten zwischen den Goldschürfern und der einheimischen Bevölkerung. [68] Es gibt jedoch erste Projekte ökologischen Goldabbaus, wie das Oro Verde in Kolumbien. Für Barren, deren Gold aus dieser Mine stammt, wurde im Februar 2011 erstmals das Fair-Trade-Siegel vergeben. [69] Europas erste Lieferanten für Faires Gold waren in Frankreich und Großbritannien, seit einiger Zeit ist es auch in Österreich erhältlich.
Eigenschaften
Physikalische Eigenschaften
Gold besteht aus nur einem stabilen Isotop , gehört damit zu den 22 Reinelementen und lässt sich leicht mit vielen Metallen legieren . Das Schwermetall ist unlegiert weich wie Zinn mit einer Mohshärte von 2,5 bis 3 ( VHN 10 = 30–34; silberhaltig 44–58 [7] ).
Gold lässt sich aufgrund seiner unerreichten Duktilität und Dehnbarkeit zu hauchdünnem Blattgold schlagen und zu besonders dünnen Folien von etwa 2000 Atomlagen und 100 Nanometern Stärke auswalzen. Dies entspricht nur ca. 1/10 der Wellenlänge des roten Lichtes und ergibt eine durchscheinende Folie, die im Durchlicht blaugrün erscheint. Ernest Rutherford verwendete Goldfolie für seinen Streuversuch . Aus einem Gramm Gold kann ein 24 km langer Faden gezogen werden. [32]
Gold kristallisiert ausschließlich in einemkubisch flächenzentrierten Raumgitter und weist damit eine kubisch dichteste Kugelpackung mit der Raumgruppe Fm 3 m (Raumgruppen-Nr. 225) auf. Der Gitterparameter beträgt bei reinem Gold 0,4078 nm [70] (entspricht 4,078 Å ) bei 4 Formeleinheiten pro Elementarzelle . [71]
Bei Versuchen in der Hochdruckforschung konnte allerdings nachgewiesen werden, dass Gold bei sehr schnell erfolgender Kompression eine andere Struktur annimmt und sogar flüssig wird. Während der Hochdruckversuche wurden kleine Goldproben mithilfe von Laserschocks innerhalb von Nanosekunden extrem stark zusammengepresst. Ab 220 Gigapascal wandelt sich dabei die kubisch flächenzentrierte Struktur in die weniger kompakte kubisch-raumzentrierte Struktur . Bei weiterer Erhöhung des Drucks auf 330 Gigapascal beginnt das Gold zu schmelzen. Der Theorie des Forschungsleiters Richard Briggs vom Lawrence Livermore National Laboratory zufolge soll Gold einen Tripelpunkt oberhalb von etwa 220 Gigapascal haben, bei dem die flächenzentrierte, raumzentrierte und flüssige Phase nebeneinander existieren können. [72]
Reines Gold hat eine metallisch-sattgelbe Farbe, die entsprechend als „goldgelb“ bekannt ist und eine ebensolche Strichfarbe . In feiner Verteilung ist es je nach Korngröße gelblich, ockerbraun bis purpurviolett und wird dann als Goldpurpur bezeichnet. Mit zunehmender Temperatur verliert Feingold an Farbintensität und ist hellgelb glühend bevor es schmilzt. Das geschmolzene Metall ist zitronengelb, leicht grünlich und erhält seine intensive gelborange Farbe erst wieder, wenn es vollständig abgekühlt ist. Vor dem Lötrohr ist Gold leicht schmelzbar zu einer vollkommenen Kugel. [73]
Beimengungen von Kupfer lassen es rosa oder rötlich erscheinen, senken die Schmelztemperatur und steigern zugleich Härte, Festigkeit und Polierbarkeit beträchtlich. Steigende Silberanteile verändern die Farbe des reinen Goldes über hellgelb nach hellgrün und schließlich zu weiß; Schmelztemperatur und Härte verändern sich dabei nur sehr wenig. Die meisten Metalle, so auch die bekannten Platinmetalle , Quecksilber und die Eisenmetalle , führen als Beimischungen dagegen in steigenden Anteilen zu einer Entfärbung in Form einer eher schmutziggelbgrauen bis grauweißen Legierung. So variiert die Farbe von palladiumhaltigem Gold (Porpezit) zwischen lohfarben und hellbraun. [74]
Einige der ungewöhnlichen Eigenschaften wie die goldgelbe Farbe und hohe Duktilität werden aktuell mit dem Einfluss von relativistischen Effekten auf die Elektronenorbitale erklärt. So entsteht die gelbliche Farbe durch Absorption im Frequenzbereich der Komplementärfarbe Blau. Ursache dafür ist die auf Grund relativistischer Effekte vergleichsweise kleine Bandlücke zwischen dem 6s- und den 5d- Orbitalen . [75] [76] [77] Während energiereiche blaue Photonen absorbiert werden und zu Elektronenübergängen führen, werden die anderen, weniger energiereichen Photonen (grün, gelb, rot) aus dem Spektrum sichtbaren Lichts reflektiert, wodurch die gelbe Färbung entsteht. [78]
In der Oberflächenchemie werden verschiedene Flächen von Au- Einkristallen ua in der Rastertunnelmikroskopie eingesetzt (siehe Abbildung). [79]
Die spezifische Verdampfungsenthalpie ΔH v von Gold ist mit 1,70 kJ/g wesentlich geringer als beispielsweise diejenige von Wasser (mit 2,26 kJ/g) oder Eisen (6,26 kJ/g, alle für die Siedetemperatur bestimmt). Bei überhitzten Goldschmelzen können daher (wie auch bei anderen Schmelzemanipulationen etwa in der Stahlindustrie ) beträchtliche Rauch- und Verdampfungsverluste auftreten, sofern der Schmelzvorgang ohne Abdichtung oder Absaugung und Abscheidung in Aktivkohle erfolgt. [80]
Chemische Eigenschaften
Gold wird von gewöhnlichen (Mineral-)Säuren nicht angegriffen. Lediglich einige stark oxidierende Säuren wie Königswasser (einem Gemisch aus Salzsäure und Salpetersäure ) oder Selensäure lösen Gold. In Königswasser bildet sich Tetrachloridogoldsäure :
Die Halogene Chlor , Brom und Iod vermögen Gold zu lösen, letzteres sogar in alkoholischer Lösung. In wässrigen Cyanidlösungen ist Gold leicht unter Oxidation durch Sauerstoff als Kaliumdicyanidoaurat(I) löslich . [81] [82] In heißen, sauren hydrothermalen Lösungen ist Gold relativ gut physikalisch löslich. [83] Demzufolge wird es oft in Quarzgesteinen mit vorgefunden. Es wurde beobachtet, dass einige Huminsäuren in der Lage sind, Gold anzulösen. [84]
Verwendung
Rund die Hälfte des am Markt gehandelten Goldes wird zu Schmuck verarbeitet, etwa ein Drittel wird von institutionellen und privaten Investoren erworben (ohne Zentralbanken), 9 % werden in der Industrie einschließlich Zahntechnik verwendet (Durchschnittswerte für 2010–2014). Die Aufkäufe durch Zentralbanken haben stark zugenommen: von 2 % der weltweiten Nachfrage im Jahr 2010 auf 14 % im Jahr 2014. [85]
Schmuck, Dekoration und Lebensmittelzusatzstoff
Der größte Teil des gewonnenen Goldes wird in der Schmuckindustrie verwendet. Goldschmiede verarbeiten Gold und andere Edelmetalle zu Ringen, Ketten, Armbändern und anderem Schmuck . Der Edelmetallgehalt wird durch die Repunze beglaubigt. Einige Orden sind aus Gold gefertigt ( Kutusoworden ). Indien und China sind die beiden größten Märkte für Goldschmuck, zusammen sorgen sie für über 50 % der Nachfrage nach Gold in diesem Bereich. [86]
Goldfolie, auch Blattgold genannt, gibt nichtmetallischen Gegenständen, wie Bilderrahmen , Büchern ( Goldschnitt ), Mobiliar, Figuren, Architekturelementen, Stuck und Ikonen das Aussehen von echtem Gold. Seit der Antike wird Blattgold von Goldschlägern aus hochgoldhaltigen Legierungen hergestellt. Dabei wird Gold dünner als die Wellenlänge des sichtbaren Lichtes gewalzt und geschlagen. Im Auflicht glänzt die Folie goldgelb, im Gegenlicht scheint die Lichtquelle grünlich-blau durch und bildet das Schlagmuster des Metalls ab. Der Vergolder präpariert die Unterlage zunächst mit einem Klebemittel und legt anschließend die Goldfolie auf. Mit 1 Gramm Blattgold kann ein halber Quadratmeter Fläche überzogen werden.
Dekorativ findet Gold vielfältige Anwendungen, zum Beispiel in galvanischen Beschichtungen von Metallen und Kunststoffen. Auf Porzellanglasuren, Zahnersatzkeramiken und Glas lassen sich Goldpigmente einbrennen. Historisch war die Feuervergoldung von Metallen mit Hilfe der Gold-Quecksilber-Legierungen, sogenannter Amalgame, nachweislich schon in der Antike die einzig brauchbare Methode, um dauerhafte Vergoldungen auf Silber , Bronze oder unedlen Metallen herzustellen. Mit der Entwicklung galvanischer Vergoldungsbäder im späten 19. Jahrhundert und 20. Jahrhundert wurde dieser Bereich in den Möglichkeiten qualitativ erweitert und ersetzt.
Goldpigmente wurden historisch in der Glasherstellung seit dem 16. Jahrhundert eingesetzt ( Goldrubinglas ), werden allerdings weitgehend durch preiswertere Verfahren ersetzt.
Im Speisenbereich wird Gold als Lebensmittelzusatzstoff E 175 [87] verwendet. In Form von Blattgold und Blattgoldflocken dient es zum Vergolden von Speisen, zum Beispiel für Überzüge von Süßwaren und zur Verzierung von Pralinen. In Getränken wird es für Danziger Goldwasser und Schwabacher Goldwasser verwendet. Metallisches Gold gilt als ungiftig, reichert sich im Körper nicht an und wird mit dem Rest der verdauten Nahrung wieder ausgeschieden.
Wertanlage und Währung
Gold dient in Form von Goldmünzen und Barrengold als Wertanlage und als internationales Zahlungsmittel. Gold wird von vielen Zentralbanken der Welt als Währungsreserve eingelagert, obwohl die Währungen nicht mehr durch Goldreserven gedeckt sind.
Anlagegold
Private und institutionelle Anleger investieren in Gold und in Wertpapiere , die den Goldkurs abbilden. In Krisenzeiten ( Inflation oder Wirtschaftskrise ) wird Gold als stabile Wertanlage gesehen, die Wertsteigerungen relativ zu anderen Wertanlagen erfahren kann. Gold hat kein Ausfallrisiko wie die meisten anderen Geldanlagen, bei denen sich die Verzinsung unter anderem nach dem wahrgenommenen Ausfallrisiko der Marktteilnehmer richtet. Bei dieser Betrachtung ist allerdings zu beachten, dass der Goldpreis im Zeitablauf starken Schwankungen ausgesetzt ist.
Goldpreis
Der Preis des Goldes wird auf dem offenen Markt bestimmt. Das geschieht seit dem 17. Jahrhundert am London Bullion Market . Seit dem 12. September 1919 treffen sich wichtige Goldhändler in einer Rothschild-Bank in London, um den Goldpreis formal zu fixieren (siehe Goldfixing ). Seit 1968 gibt es ein weiteres tägliches Treffen in der Bank um 15 Uhr Londoner Zeit, um den Preis zur Öffnungszeit der US-Börsen erneut festzulegen. Für den standardisierten Goldhandel an Rohstoffbörsen wurde „ XAU “ als eigenes Währungskürzel nach ISO 4217 vergeben. Es bezeichnet den Preis einer Feinunze Gold.
Am 17. März 1968 wurde der Goldpreis gespalten und ein zweigliedriges System eingeführt. Der eine Preis konnte sich frei dem Markt anpassen, der andere war fix. 1973 wurde der Goldpreis freigegeben, und der Besitz von Gold war in den USA wieder erlaubt. China hat den Privatbesitz von Gold 1983 wieder erlaubt (siehe Goldverbot ).
Der Goldpreis ist unter anderem von den aktuellen Fördermengen, vom Ölpreis und vom Kurs des US-Dollars abhängig, da Gold zumeist in US-Dollar gehandelt wird. Er kann von den Zentralbanken beeinflusst werden, die zusammen etwa 30.750 Tonnen Gold besitzen (Stand Dezember 2011), [88] das sind knapp 19 % der weltweit vorhandenen Goldmenge von 170.000 Tonnen. [89]
Gold als Währung oder Währungsdeckung
Historisch wurde Gold seit Jahrtausenden als Währung eingesetzt. Eine Geldeinheit entsprach einer bestimmten Menge Gold. In Deutschland war während des Deutschen Reichs von 1871 bis 1918 das gesetzliche Zahlungsmittel die Goldmark (siehe auch Kurantmünze ), wobei 2,79 Goldmark einem Gramm Gold entsprachen und die Reichsbank gegen Vorlage einer Banknote die entsprechende Menge in physisches Gold eintauschte. Die Golddeckung wurde zu Beginn des Ersten Weltkrieges aufgehoben; und konnte danach nicht wieder eingeführt werden wegen der Reparationen, die die Goldreserven des Deutschen Reiches verschlangen, und wegen der Vervielfachung der in Umlauf gebrachten Papiergeldmenge. Diese faktische Umstellung auf nicht-goldgedecktes Geld (Vertrauenswährung oder Fiat Money ) führte bereits während des Krieges zur Abwertung der Mark und ermöglichte die Hyperinflation der 1920er Jahre.
Lange Zeit entsprachen in den Vereinigten Staaten 20,67 US-Dollar einer Unze Gold. 1934 fand eine Abwertung des US-Dollars durch die Neufestlegung des Goldpreises auf 35 US-Dollar je Feinunze statt. [90] Das neue Verhältnis wurde im Bretton-Woods-System von 1944 bestätigt.
Um Gold als Währungsalternative auszuschließen und um die Währungsreserven ( Goldreserve ) zu erhöhen, war der Goldbesitz in den USA zeitweise verboten. Von 1933 bis 1973 war Goldbesitz nur in Form von Schmuck und Münzsammlungen erlaubt. Präsident Franklin D. Roosevelt ließ Gold über die Executive Order 6102 konfiszieren. Präsident Richard Nixon beendete 1971 das Bretton-Woods-System und schaffte dessen Versprechen ab, dass alle Nationalbanken eine Feinunze Gold für 35 US-Dollars von der US-Notenbank verlangen können.
Da der Goldstandard die herausgegebene Geldmenge und die Höhe der Staatsverschuldung beschränkt, waren die Regierungen daran interessiert, ihre Währungen vom Gold zu lösen. In beiden Weltkriegen wurde der Goldstandard aufgegeben, da die benötigten Geldmittel zur Kriegsproduktion nur per Inflation aufzubringen waren. Heutzutage sind sämtliche Währungen der Welt vom Gold losgelöst, und erst dadurch war die extreme Ausweitung der heutigen Geldmengen und Schulden möglich. Die vorhandene Goldmenge würde zu den aktuellen Kursen nicht als Wertdeckung für eine bedeutsame Währung ausreichen. Das im Januar 2006 vorhandene Gold entsprach einem Marktwert von 2,5 Billionen € und wäre hypothetisch somit gerade einmal geeignet gewesen, die damaligen Staatsschulden Deutschlands und Spaniens zu decken. Im Falle einer erneuten Deckung von bedeutenden Währungen müsste der Goldkurs auf ein Vielfaches ansteigen.
Elektronik
Die Elektronikindustrie verwendet Gold ua aufgrund der guten Verarbeitbarkeit und hervorragenden Kontaktgabe (hohe Korrosionsbeständigkeit, leichte Lötbarkeit): [91]
- Bonden:
- Bonddrähte (Verbindungsdrähtchen zwischen den Chips und den Anschlüssen Integrierter Schaltkreise ) sowie Bondinseln und Leiterstrukturen werden teilweise aus reinem Gold gefertigt: ein Gramm lässt sich zu einem Bonddraht von mehr als drei Kilometern Länge ziehen. Aus Kostengründen werden zunehmend Bonddrähte aus Aluminium oder Kupfer eingesetzt.
- Die Montage ( Chipbonden ) von mikroelektronischen und Laserdioden-Chips erfolgt auf vergoldeten Flächen
- Leiterplatten (ihre Kupferleiterbahnen und Kontaktierungsstellen) mit Direkt-Steckverbindern werden häufig vergoldet
- Schaltkontakte für Signalschalter und Relais
- Vergolden von Steckverbindern und Kontaktflächen („Hauchvergolden“ oder bis 1 µm Schichtdicke)
Medizin
Wegen seiner Korrosionsbeständigkeit und ästhetischen Qualitäten wird es in der Zahnprothetik als Füll- oder Ersatzmaterial für defekte oder fehlende Zähne eingesetzt. Dabei kommen Legierungen zum Einsatz, da reines Gold zu weich wäre. Diese bestehen meist zu rund 80 % aus Gold und zu 20 % aus Beimetallen wie Platin . Die Popularität von Goldzähnen hat in westlichen Ländern zugunsten unauffälligerer Kunststoffimplantate abgenommen, während sie in vielen anderen Teilen der Erde nach wie vor häufig verwendet werden.
Einige Goldsalze werden (intramuskulär verabreicht) heilend zur Rheumatherapie eingesetzt, etwa Aurothioglucose (Aureotan) [92] als langsamwirkendes Langzeittherapeutikum. Die Goldsalze Natriumaurothiomalat und Auranofin werden als Basismedikamente gegen rheumatoide Arthritis (chronische Polyarthritis) angewendet. Goldtherapien erreichen ihre volle Wirkung erst nach mehreren Monaten und sind mit Nebenwirkungen verbunden. Es kann zu allergischen Reaktionen und bei unsachgemäßer Anwendung zu einer Schädigung von Leber, Blut und Nieren kommen. Etwa 50 % der Therapien mit Goldsalzen werden aufgrund der unerwünschten Wirkungen abgebrochen. In neuerer Zeit verdrängen preisgünstigere Medikamente mit besserem Nebenwirkungsprofil die Behandlung mit goldhaltigen Therapeutika.
1913 ließ der Arzneimittelhersteller Madaus das homöopathische Präparat Essentia Aurea: Goldtropfen patentieren, das unter der Marke „Herzgold“ verkauft und gegen Herz- und allgemeine Schwächezustände angewandt wurde. [93]
Seit dem Mittelalter waren, zuerst bei den Arabern, wohl auch vergoldete Pillen in Gebrauch. [94] Meist wurden unter „Goldenen Pillen“ ( pillae aureae , pillulae aureae , güldîn körnlîn [95] ) jedoch aus verschiedenen Zutaten hergestellte Pillen bezeichnet, die im salernitanischen Antidotarium Nicolai aufgeführt und als „wertvoll wie Gold“ angeboten wurden. [96]
Um 1935 wurden Versuche unternommen, die vor Einführung der Antibioka wenig erfolgreiche Syphilis -Therapie durch Anwendung von Goldpräparaten zu verbessern. [97]
Mitte der 1970er Jahre entwickelte der amerikanische Tierarzt Terry Durkes [98] die Goldimplantation zur Schmerztherapie arthrotischer Gelenke bei Hunden und Pferden, die seit 1996 auch in der Humanmedizin als alternativmedizinisches Verfahren angewandt wird. [99] Ein wissenschaftlicher Wirkungsnachweis liegt nicht vor, das Verfahren ist in keiner Leitlinie genannt.
Optik
Gold reflektiert Infrarotlicht sehr gut (98 % bei Wellenlängen > 700 nm) [100] sowie rotes und gelbes Licht besser als blaues und violettes. Deshalb werden wärmereflektierende Beschichtungen auf Gläsern, Strahlteilern und Spiegeln – auch Laserspiegel für Laser im mittleren Infrarot – sowie auf Hitzeschutzvisieren (Feuerwehr, Gießereien und so weiter) aus Goldschichten hergestellt ( Sputtern , Bedampfen , mit Schutzschicht).
Gold ist ein Dotand von Germanium (Germanium-Gold, kurz Ge:Au) – einem Halbleiter zum Nachweis von Infrarot von 1 bis etwa 8 µm Wellenlänge bei Kühlung auf 77 K nach dem Prinzip der Photoleitung .
Nanopartikel
Nanoskopisch vorliegende metallische Goldpartikel, also solche mit einer Größe im Nanometer -Maßstab, sind in jüngster Zeit Schwerpunkt intensiver Forschung geworden, weil ihre Verwendung als heterogene Katalysatoren in organisch-chemischen Reaktionen neue, lösungsmittelfreie Verfahren zulässt. Dies ist Teil eines Prozesses der Umgestaltung der chemischen Produktionsweisen in Richtung einer grünen Chemie . Weiterhin werden Gold-Nanopartikel als inertes Trägermaterial mit verschiedenen Molekülen beschichtet, [101] etwa zur Verwendung in einer Genkanone .
In diesem Zusammenhang wurde entdeckt, dass Gold-Nanopartikel nach Adsorption chiraler Substanzen selbst chirale Strukturen aufweisen können. [102] Die Chiralität dieser Partikel kann durch die Enantiomere der Adsorbentien gesteuert werden, bleibt jedoch erhalten, wenn in achiraler ( racemischer ) Umgebung verfahren wird. [103]
Reinheit und Echtheit
Feingehalt
| Karat |
Gewichtspromille Gold in der Legierung |
im Handel als | Atom % ca. |
|---|---|---|---|
| 24 kt | 999 | Feingold 999 | 100 |
| 22 kt | 916 2 ⁄ 3 | Gold 916 | 83 |
| 20 kt | 833 1 ⁄ 3 | Gold 833 | 68 |
| 18 kt | 750 | Gold 750 | 50 |
| 14 kt | 583 1 ⁄ 3 | Gold 585 | 38 |
| 10 kt | 416 2 ⁄ 3 | Gold 417 | 23 |
| 9 kt | 375 | Gold 375 | 20 |
| 8 kt | 333 1 ⁄ 3 | Gold 333 | 18 |
Die Reinheit von Gold wird historisch in Karat (abgekürzt kt) angegeben. 24 Karat entsprechen purem Gold (Feingold). Mit Einführung des metrischen Systems wurde die Umstellung auf Promille-Angaben vorgenommen. So bedeutet der Stempeleindruck „750“ in Goldware, dass das Metall von 1000 Gewichtsanteilen 750 Anteile (dh 3 ⁄ 4 ) reines Gold enthält, entsprechend 18 Karat („585“ entspricht 14 Karat, „375“ entspricht 9 Karat und „333“ entspricht 8 Karat). Bullionmünzen haben entweder 916,6 Promille ( Krugerrand , Britannia , American Eagle ) oder 999,9 Promille Gold ( Wiener Philharmoniker , Maple Leaf , Nugget , American Buffalo ). Die Reinheit kann mit einer Dezimalzahl angegeben werden, zum Beispiel als 0,999 oder 1,000 (Feingold).
Hochwertiger Schmuck wird international üblicherweise aus Goldlegierungen mit einem Feingehalt von 750 oder höher angefertigt. Dabei ist die Wahl des verwendeten Feingehaltes von regionalen und kulturellen Vorlieben beeinflusst. So werden auf dem amerikanischen Kontinent vor allem Legierungen mit 585 ‰ Goldanteil verwendet, während im Nahen Osten sattgelber Goldschmuck ab Feingehalten von etwa 20 bis 22 kt (833–916 ‰) aufwärts besonders geschätzt wird. In Südostasien und im chinesisch, thailändisch und malaiisch beeinflussten Kulturkreis geht dies traditionell sogar bis hin zum Schmuck aus reinem Feingold, der in der dortigen Kultur als besonders hochwertig betrachtet wird.
Die Anteile an eventuell enthaltenen anderen Edelmetallen ( Silber , Palladium , Platin , Rhodium , Iridium ua) wird bei der Stempelung nicht berücksichtigt.
Goldimitate
Vor allem aufgrund des hohen Preises von Gold wurden Legierungen aus unedlen Metallen entwickelt, die als Goldimitat benutzt werden oder als Unterlage bei der Herstellung von Doublé Verwendung finden. [104] Dies sind in den meisten Fällen ungenormte Kupferlegierungen mit den verschiedensten Zusätzen. Eine Legierung aus mindestens 50 % Kupfer und Zink als Hauptlegierungsanteil (bis über 44 %) ist als Messing bekannt. Die Zugabe von Blei (bis zu 3 %) erhöht die Zerspanbarkeit des Messings. Wichtige Messingsorten sind Tombak (über 67 % Kupfer) und Sondermessing (enthält weitere Metalle).
Aus Edelmetallen werden Legierungen hergestellt, die wie Gold erscheinen können, ohne dass Gold in ihnen enthalten ist. Bei manchen Legierungen wird jedoch Gold selbst in geringen Anteilen hinzugegeben.
Prüfmethoden
Die Prüfung von Gold auf dessen Echtheit und Reinheit und somit die Wertbestimmung erfolgt durch verschiedene Methoden:
- Wiegen nach Archimedischem Prinzip : Feststellung des spezifischen Gewichts durch die Messung von verdrängtem Wasser und Vergleich mit offiziellen Listen. Eine einfache Methode, die aber nur mit einer Feinwaage exakt ist. Zudem gibt es Abweichungen bei stark zerklüfteten und unregelmäßig geformten Goldstücken.
- Strichprobe und Säuretest: Probierstriche werden mit Probiersäuren (meist Salpetersäure) in unterschiedlicher Konzentration betupft. Mit dieser Methode behelfen sich Goldschmiede, Münzsammler zur annähernden Bestimmung des Feingehaltes im Alltag. Beim Säuretest muss ein Teil des Prüflings abgerieben werden, so wird ein Materialverlust in Kauf genommen.
- Röntgenfluoreszenzspektrometer : Abtastung mit Röntgenstrahlen im Labor und Auswertung mit einem Computerprogramm. Sehr exakte Bestimmung des Feingehalts von Edelmetallen ohne Materialverlust, jedoch muss die notwendige Ausstattung vorhanden sein.
- Leitfähigkeitsanalyse mit der Wirbelstromprüfung : Mit Hilfe einer Spule wird ein wechselndes Magnetfeld erzeugt, welches Wirbelströme im Material induziert. Ein Sensor misst die elektrische Leitfähigkeit im Inneren des Metalles, welche mit dem Sollwert abgeglichen wird. Dies ist eine zerstörungsfreie Methode, um auch Münzen oder kleine Barren überprüfen zu können. [105]
- Magnetwaage : Gold wird als diamagnetisches Material von einem externen Magnetfeld abgestoßen. Diese Kräfte lassen sich am besten mit einer Magnetwaage messen, wodurch man z. B. Gold von Wolfram-Imitaten unterscheiden kann, die sich paramagnetisch verhalten und damit in das Magnetfeld hineingezogen werden. [106]
Goldlegierungen
Allgemeines
Klassische Goldlegierungen für Schmuck gehören dem Dreistoffsystem Gold-Silber-Kupfer an. Ein Grund dafür ist, dass diese Metalle natürlich miteinander vorkommen und es bis ins 19. Jahrhundert in Europa verboten war, Gold mit anderen Metallen als Kupfer und Silber zu legieren. Das Farbspektrum derartiger Goldlegierungen reicht von sattgelb über hellgrün und lachsrosa bis hin zu silberweiß. Diese Legierungen sind leicht herstellbar und gut zu verarbeiten. Je nach Anforderung werden durch Zusatz weiterer Metalle die Legierungseigenschaften wie erwünscht beeinflusst. So senken beispielsweise kleinere Zusätze von Zink , Indium , Zinn , Cadmium oder Gallium die Schmelztemperaturen und die Oberflächenspannung der Metallschmelze bei nur geringfügiger Änderung der Farbe der Legierung. Dies ist eine Eigenschaft, die der Verwendung als Lotlegierungen für andere Goldwerkstoffe entgegenkommt. Andere Zusätze wie Platin , Nickel oder höhere Kupferanteile erhöhen beträchtlich die Härte der Metallmischung, verändern aber die schöne Farbigkeit des Goldes negativ. Zusätze wie Blei (bleihaltiges Lötzinn) , Bismut und viele Leichtmetalle machen Goldlegierungen spröde, sodass diese nicht mehr verformbar sind.
Doch nicht nur die Art, sondern auch die Menge der zugesetzten Metalle verändert die Goldlegierungen in gewünschter Weise. Ist eine satte Eigenfarbe erwünscht, sind bei sehr edlen Goldlegierungen mindestens drei Viertel Massenteile Gold erforderlich. Höchste Festigkeit und Härte werden bei den eher blasseren Goldlegierungen mit einem Feingehalt um 585 erreicht, weshalb dieses empirisch gefundene Legierungsverhältnis seit langem verwendet wurde. Legierungen mit einem deutlich geringeren Feingehalt als diese sind hingegen aufgrund der unedlen Beimischungen durch langfristige Korrosionseffekte bedroht.
Weiterhin ist zu unterscheiden, ob die Legierungen als Gussmaterial verarbeitet werden sollen oder wie herkömmlich als Knetlegierungen , also schmiedbar, zur Kaltverformung geeignet sein müssen. Erstere beinhalten Kornfeinungszusätze im Zehntelpromillebereich, die beim langsamen Erstarren der Schmelze in der Gussform das Kristallwachstum günstig beeinflussen, Zusätze von etwas Silicium unterdrücken die Oberflächenoxidation beim Erhitzen in der Luft, verschlechtern aber die Kaltbearbeitungsfähigkeit und Lötbarkeit.
Legieren bedeutet in diesem Zusammenhang letztendlich ein „Verdünnen“ des reinen Goldes und es werden seine geschätzten Eigenschaften wie Farbe, Korrosionsfestigkeit , Preis, Dichte „verdünnt“, doch gewinnt mechanische Festigkeit und Polierfähigkeit hinzu.
Edelmetallanteile und Korrosionsfestigkeit
Die gebrauchsfreundlichen Eigenschaften, das „Edle“ der Goldlegierungen, wird durch das Verhältnis von Edelmetallatomen zur Gesamtanzahl der Atome in der Legierung bestimmt. Deren Eigenschaften wie Korrosionsfestigkeit, Farbwirkung oder intermetallische Bindung werden durch dieses Stückzahlenverhältnis festgelegt. Die Stoffmenge, das Mol und die Stöchiometrie weisen darauf. Der Gewichtsanteil bestimmt nur indirekt die Eigenschaften und ist darüber hinaus sehr von den verwendeten Zusatzmetallen abhängig.
Gold mit der Atommasse 197 und Kupferatome mit der Massenzahl 63 (nur rund ein Drittel) bilden eine Legierung mit dem Atomverhältnis 1:1. Dieses Legierungsbeispiel zeigt ein Gewichtsanteil von 756 Teilen Feingold und suggeriert über das Gewicht einen hohen Edelmetallgehalt. Genau betrachtet jedoch beträgt dieser über den Anteil der Goldatome (die Stückzahl) nur 50 %. Empirisch wird jedoch eine Legierung unter 50 Atomprozent Gold von Säuren angreifbar. Je kleiner die Atommassen der Legierungszusätze, desto drastischer fällt dieser Effekt aus.
So betrachtet sind bei den üblicherweise verwendeten 750er-Goldlegierungen bereits nur die Hälfte der Legierungsatome Gold. Ein extremes Beispiel ist eine 333er-Goldlegierung, denn hier kommen nur 2 Goldatome auf 9 Zusatzatome. Dies erklärt die sehr unedlen Eigenschaften dieses Materials, wie hohe Anlaufneigung, Korrosionsverhalten und geringe Farbtiefe. Viele Goldschmiede und Länder, wie die Schweiz, lehnen es ab, diese Legierung noch als „Gold“ aufzufassen.
Farbgoldlegierungen
Die Zahlangabe 750/ooo – egal ob bei Weißgold, Rotgold oder Gelbgold – besagt immer, dass dieselbe Menge Feingold in der jeweiligen Legierung enthalten ist. Kupfer, Silber oder Palladium und andere Legierbestandteile wechseln jedoch – je nach Farbe der Goldlegierung – in ihrer mengenmäßigen Zusammensetzung.
Rotgold
Rotgold ist eine Goldlegierung, bestehend aus Feingold, Kupfer und gegebenenfalls etwas Silber, um die mechanische Verarbeitbarkeit zu verbessern. Der relativ hohe Kupferanteil, der deutlich über dem des Silbers liegt, ist für die namensgebende „rote“ Färbung und Härte des Materials verantwortlich. Der Farbton ist kupferähnlich.
Regional sind bestimmte Goldfarbtönungen beliebt; so werden im Osten und Süden Europas eher dunklere und farbstarke rötlichere Goldlegierungen verwendet. Umgangssprachlich wurde Rotgold in der DDR als Russengold bezeichnet; teilweise ist in Süddeutschland noch der Begriff Türkengold gebräuchlich. Russengold hat den ungebräuchlichen Feingehalt von 583 und ist daran sehr gut zu erkennen. Die Färbung ist etwas heller als beim Rotgold. Helles, ins Rosa gehendes Gold mit geringem Kupferanteil, das dafür neben Silber auch Palladium enthalten kann, wird als Roségold angeboten.
Gelbgold
Dabei handelt es sich um eine dem Feingold ähnelnde gelbe Goldlegierung aus Feingold mit Silber und Kupfer. Das Verhältnis beeinflusst die Farbe. Mit abnehmendem Goldgehalt reduziert sich die Tiefe des Gelbtons sehr schnell. Üblicherweise ist das Verhältnis der dem Gold zugesetzten Metalle untereinander ca. 1:1; die Tönungen und Farbintensität können stufenlos und beliebig gewählt werden. Die Farbe reicht von hellgelb mit deutlichem Silberanteil bis zu gelborange mit dem umgekehrten Verhältnis zum Kupferzusatz. Gelbgold ist durch ihren hohen Erkennungswert weltweit mit Abstand die beliebteste Goldfarbe.
Grüngold
Grüngold ist eine grünlichgelbe Goldlegierung ohne Kupferzusatz. Die Farbe entsteht durch Annäherung an das Atomverhältnis Gold:Silber 1:1, was im optimalen Fall einem Goldanteil von 646 entspricht, bei dem der deutlichste Grünton auftritt. Da in diesem Falle der Silberanteil schon über 40 % beträgt, ist der Farbton relativ hell. Bis zu einem Drittel des Silbers lässt sich durch Cadmium ersetzen, was den Grünton intensiviert, die günstigen Anlaufeigenschaften und die Schmelztemperatur allerdings reduziert. Die Legierungen sind sehr weich und wenig farbstark. Grüngold wird selten verwendet, üblicherweise zur Darstellung von Laubblättern oder ähnlichem.
Weißgold und Graugold
Weißgold als Sammelbegriff bezeichnet Goldlegierungen, die durch Beimischung deutlich entfärbender Zusatzmetalle eine weiß-blassgetönte Goldlegierung ergeben. Als Legierungszusätze werden hauptsächlich das Platinnebenmetall Palladium , (früher sehr häufig) Nickel oder bei niedrigen Goldgehalten Silber verwendet. Die Entfärbung des von Natur aus gelben Goldes tritt kontinuierlich ein und setzt eine gewisse Menge des entfärbenden Zusatzes voraus; der Rest, der dann noch bis zum berechneten Gesamtvolumen fehlt, wird oft aus Kupfer oder Silber gestellt.
Im frankophonen Sprachraum sind diese Werkstoffe treffender als or gris , „Graugold“, bekannt.
Viele Metalle bilden mit Gold „weiße“ Legierungen, so Quecksilber oder Eisen (durch die Legierung mit dem Edelmetall Gold wird Eisen nicht rostfrei ). Platin bildet mit Gold eine schwere, teurere und sehr gut aushärtbare Legierung. Die in präkolumbischer Zeit in Südamerika hergestellten Platinobjekte bestehen aus diesem weißlich-beige bis schmutzig-grau aussehenden Material.
Nickelhaltiges Weißgold (eine Gold-Kupfer-Nickel-Zink-Legierung mit variablen 10–13 % Nickelanteil) kann als durch den Nickel zusatz entfärbte Rotgoldlegierung aufgefasst werden; demzufolge ist es relativ hart und kann bis zur Federhärte gewalzt, gezogen oder geschmiedet werden. Die hohe Grundfestigkeit ermöglicht beispielsweise geringere Wandstärken bei gleicher Stabilität. Weitere Eigenschaften wie hervorragende Zerspanbarkeit und Polierbarkeit sind von großem Vorteil. Dazu kommen noch der niedrige Schmelzpunkt und günstigere Preis, der wiederum daraus resultiert, dass keine weiteren Edelmetalle im Zusatz enthalten sind und die Dichte geringer ist als beim palladiumlegierten Pendant. Für mechanisch beanspruchte Teile wie Broschierungen, Nadeln, Scharniere und Verbindungsteile wird dieses Material von den Schmuckherstellern und Juwelieren aufgrund der Festigkeit sehr geschätzt. Nickelweißgold ist die Basis von weißgoldenen Lotlegierungen. Da jedoch der Nickelanteil auf der Haut allergische Reaktionen hervorrufen kann, wird es mittlerweile in fast allen modernen Schmucklegierungen weitestgehend vermieden.
Die edlere Alternative ist palladiumhaltiges Weißgold , eigentlich treffender als Graugold zu bezeichnen. Es ist vergleichsweise weich, wobei es unterschiedliche Rezepturen von harten bis weichen Legierungen gibt. Es handelt sich um Mehrstofflegierungen mit bis zu sechs Komponenten. Der Grundfarbton der palladiumbasierten Goldmischungen ist allgemein dunkler, eben „grauer“ als der des nickelbasierten Weißgoldes. Der Palladiumzusatz mit ca. 13–16 % muss höher als beim Nickelweißgold gewählt werden, um die Gesamtmischung vergleichbar zu entfärben. Üblicherweise werden diese Weiß-/Graugoldlegierungen nach der Bearbeitung meist rhodiniert . Daher ist es weniger wichtig, dass die Legierung ganz farbrein weiß oder hellgrau erscheint, und es wird bewusst am Palladiumzusatz gespart, welcher den Preis deutlich auftreibt und zudem die Mischung nachteilig dunkler färbt. Nativ sehen diese Werkstoffe demzufolge oft leicht beige aus. Der Vergleich mit Platin oder Silber ist augenfällig. Die Verarbeitungseigenschaften, wie Zerspanbarkeit, die bei maschinellem Drehen beispielsweise von Trauringen gefordert ist, stellen andere Anforderungen an die Werkzeuge. Die Gießeigenschaften (höherer Schmelzpunkt und höhere Oberflächenspannung der Schmelze) unterscheiden sich vom nickelbasierten Pendant. Eine strukturelle Zähigkeit der Legierungen erhöht den Aufwand der Hochglanzpolitur in ungewohnter Weise. Nachteilig ist der erhöhte Preis durch den nicht unbeträchtlichen Palladiumanteil und die höhere Dichte des Materials. Positiv zeigen die Legierungen ihren hohen Anteil an Edelmetallen (Gold-Palladium-Silber) in deren Eigenschaften. Ein Schmuckstück in Palladiumweißgold war im Januar 2007 ca. 20 % teurer als das vergleichbare aus Gelbgold bei gleichem Feingehalt.
Anbieter von Goldlegierungen entwickeln immer wieder neuartige Werkstoffe. So gibt es Weißgoldlegierungen mit Cobalt , Chrom , Mangan - Germanium und anderen Metallen. Verarbeitungsprobleme, Preisentwicklungen oder mangelnde Akzeptanz der Kunden lassen solche neuen Goldlegierungen häufig schnell wieder vom Markt verschwinden.
Da sich „weißes“ Gold nicht elektrochemisch abscheiden lässt, werden Schmuckerzeugnisse aus Weißgold in der Regel auf galvanischem Wege rhodiniert. Dieser Überzug mit Rhodium , einem Platin-Nebenmetall, bewirkt eine Farbverbesserung hin zu einem reinen, silberartigen Weiß sowie eine verbesserte Kratzfestigkeit gegenüber der unbeschichteten Metalloberfläche aus reinem Weißgold. Dieser Rhodiumüberzug muss nicht explizit angegeben werden. Durch Abtragen dieses Überzuges kommt das eigentliche Weiß- oder Graugold wieder zum Vorschein, was bei Trauringen oft zu optischen Beeinträchtigungen führt. In den letzten Jahren werden daher Weißgoldringe bewusst in ihrer Naturfarbe verkauft, um Enttäuschungen beim Verbraucher zu vermeiden.
Titan-Gold-Legierung
Eine aushärtbare Titan -Gold- Legierung mit 99 % Gold und 1 % Titan wird in der Trauringherstellung und Medizintechnik eingesetzt. Der hohe Edelmetallanteil in Verbindung mit hoher Festigkeit machen den Werkstoff interessant. Die gelbe Farbe ist vergleichbar mit der von 750 Gelbgold, jedoch „grauer“. Durch den Titanzusatz ist die Legierung beim Schmelzen sehr empfindlich und reagiert mit Sauerstoff und Stickstoff.
Verbindungen
Gold kommt in seinen Verbindungen hauptsächlich in den Oxidationsstufen +1 und +3 vor. Daneben ist −1-, +2- und +5-wertiges Gold bekannt. Goldverbindungen sind sehr instabil und zersetzen sich bei Erwärmung leicht unter Entstehung von elementarem Gold.
- Gold(III)-oxid (Au 2 O 3 ) ist aufgrund des edlen Charakters des Elements nicht durch Verbrennung mit Sauerstoff zugänglich. Stattdessen wird von in wässriger Lösung stabilem Trichlorogold-Hydrat (AuCl 3 (H 2 O)) (als Säure eigentlich mit Hydrogentrichlorohydroxidoaurat(III) H[AuCl 3 (OH)] zu bezeichnen) ausgegangen, das, mit Lauge versetzt, als Gold(III)-hydroxid ausfällt. Beim Trocknen spaltet dieses Wasser ab und ergibt Gold(III)-oxid. Oberhalb von 160 °C zerfällt das Oxid wieder in die Elemente.
- Gold(III)-chlorid (AuCl 3 ) entsteht beim Behandeln von Goldstaub mit Chlor bei ca. 250 °C [107] oder aus HAuCl 4 und SOCl 2 . Es bildet dunkelorangerote Nadeln, die in Wasser, Alkohol und Ether löslich sind. Wasser zersetzt AuCl 3 zu Hydroxotrichlorogold(III)-säure, H[Au(OH)Cl 3 ].
- Tetrachloridogoldsäure , H[AuCl 4 ] Das Tetrahydrat bildet zitronengelbe, lange, an feuchter Luft zerfließliche Kristallnadeln, die sich in Wasser und Alkohol sehr leicht lösen; bei Lichteinwirkung treten violettbraune Flecken auf. HAuCl 4 entsteht, wenn die braunrote Gold(III)-chlorid-Lösung mit Salzsäure versetzt wird oder Gold in Königswasser gelöst und mit Salzsäure eingedampft wird. Es wird in der Medizin als Ätzmittel sowie in der Photographie (Goldtonbäder) und in der Galvanotechnik ( Vergoldung ) verwendet. Das Goldchlorid des Handels ist meist HAuCl 4 , das gelbe „Goldsalz“ dagegen Natriumgoldchlorid, Na(AuCl 4 ) · 2 H 2 O.
- Gold(I)-sulfid und Gold(III)-sulfid
- Goldcyanide, Natrium- bzw. Kaliumdicyanidoaurat(I) , (Na- bzw. K[Au(CN) 2 ]), die beim Vergolden und in der Cyanid-Laugerei eine Rolle spielen. Gewonnen werden sie durch Auflösen von Gold in einer Kalium- oder Natriumcyanidlösung:
- Eine ähnliche Reaktion tritt auf, wenn Gold in einer Thioharnstofflösung gelöst wird. Beispiel anhand der Abwasseraufbereitung:
- Caesiumaurid ist ein Beispiel für Gold als Anion mit der formalen Oxidationsstufe −1: CsAu = Cs + Au −
- Gold(V)-fluorid ist ein Beispiel für eine Goldverbindung, die Gold in der Oxidationsstufe +5 enthält.
- Gold(II)-sulfat , AuSO 4 , ist eine der wenigen Verbindungen mit Gold in der Oxidationsstufe +2. [108]
- In der Biologie wird Gold-Thioglucose verwendet, um bei Nagetieren experimentell Fettleibigkeit auszulösen.
Goldverbindungen können aufgrund der Giftigkeit des Verbindungspartners zum Teil sehr giftig sein, etwa Tetrachloridogoldsäure und die Goldcyanide.
Biologische Bedeutung
Gold und Goldverbindungen sind für Lebewesen nicht essentiell. Da Gold in Magensäure unlöslich ist, ist beim Verzehr (etwa als Dekoration) von reinem, metallischem Gold keine Vergiftung zu befürchten. Reichern sich hingegen Gold-Ionen, zum Beispiel bei übermäßiger Aufnahme von Goldsalzen, im Körper an, kann es zu Symptomen einer Schwermetallvergiftung kommen. Die meisten Pflanzenwurzeln werden durch Gabe (hoher Mengen) an Goldsalzen geschädigt.
Es gibt Menschen, die allergisch auf Goldlegierungen reagieren (Nachweisversuche mittels Natriumthioaurosulfat sind schwierig und unsicher). Diese Goldallergie ist allerdings extrem selten und noch nicht ausreichend untersucht. Bei der Verwendung von Goldfüllungen und anderem goldhaltigen Zahnersatz ist zu beachten, dass Goldlegierungen andere Bestandteile enthalten und eine allergisierende Wirkung meist von anderen Bestandteilen, beispielsweise Zink , ausgelöst werden kann. [109]
Metaphorische Verwendung und Symbolik
Mit Gold, das für wertvoll und kostbar steht, werden andere wertvolle Sachen ebenfalls bezeichnet. Meist wird ein Adjektiv hinzugesetzt, wie „Schwarzes Gold“ für Öl. Wörter und Redewendungen, in denen Gold vorkommt, sind zudem in ihrer Bedeutung meist positiv oder euphemistisch besetzt.
Beispiele:
- Schwarzes Gold – Öl , Kohle , Reifen (Rennsport), Kaviar , Shakudō , Kaffee , Sklaven , Trüffel
- Weißes Gold – Marmor , Speisesalz , Kokain , Baumwolle , Porzellan , Elfenbein , Spargel
- Blaues Gold – Trinkwasser (in wasserarmen Gebieten)
- Rotes Gold – Wein , Safran , Tomate
- Grünes Gold – Zuckerrohr , Jade
- Flüssiges Gold – Honig , Whisky , Bier
- Gold des Meeres (Meeresgold) – Korallen
- Gold des Nordens – Bernstein
- Ackergold – Kartoffel
- Katzengold oder Narrengold – Pyrit
- Trompetengold – scherzhafte Bezeichnung für Messing
- Nasengold – Kokain , Nasensekret (Popel)
- Hüftgold – kalorienreiche Nahrungsmittel bzw. Fettpolster am Körper
- Betongold – Immobilien
- goldrichtig – absolut richtig
- sich eine goldene Nase verdienen – bei Geschäften finanziell sehr erfolgreich sein
- Goldener Oktober – milde, sonnige Wetterperiode im Oktober eines Jahres, so genannt wegen des goldgelb gefärbten Laubes .
- Herz aus (purem) Gold – Wesenszug, der durch Fürsorglichkeit, Mitmenschlichkeit und Aufopferung gekennzeichnet ist.
- goldene Hände haben – handwerklich besonders begabt sein
- goldene Mitte , Goldener Mittelweg – Kompromisslösung
- Goldener Schnitt – harmonisch wirkende Teilung einer Strecke, Rechteck mit harmonischem Seitenverhältnis
- Goldene Hochzeit
Es gibt zu diesen positiv besetzten Ausdrücken Gegenbeispiele, so sind goldene Wasserhähne nicht nur Zeichen von großem Luxus, sondern Sinnbild für Dekadenz . Als „Blutgold“ wurden illegal ausgeführte Goldmengen während des Zweiten Kongokriegs bezeichnet, mit denen die beteiligten Milizen ihre Waffenkäufe finanzierten (vgl. auch → Blutdiamanten ). [110]
Schrottsammler bezeichnen Kupfer mit „Gold“, da sie unter den gängigen Metallen für Kupfer den höchsten Preis erzielen.
Heraldik
Die heraldische Bezeichnung „Gold“ steht für Gelb (wie „Silber“ für Weiß). Gelb und Weiß werden in der Heraldik als „Metalle“ bezeichnet und sollten, wenn beide im gleichen Wappen vorkommen, durch eine „Farbe“ (etwa Rot, Blau, Grün, Schwarz) voneinander getrennt sein (siehe Tingierung ).
Siehe auch
- Gold/Tabellen und Grafiken (statistische und geographische Daten)
- Kolloidales Gold (Lösung oder Gel mit winzigen Goldpartikeln, tiefrot gefärbt)
- Goldelektrolyt
Literatur
- Andrej V. Anikin : Gold . 3., neuverfasste und erweiterte Auflage. Verlag Die Wirtschaft, Berlin 1987, ISBN 3-349-00223-4 .
- 5000 Jahre Gold und Keramik aus Afrika . Heinrich-Barth-Verlag, Köln 1989, DNB 211467049 .
- Harry H. Binder: Lexikon der chemischen Elemente – das Periodensystem in Fakten, Zahlen und Daten . Hirzel, Stuttgart 1999, ISBN 3-7776-0736-3 .
- Eoin H. Macdonald: Handbook of gold exploration and evaluation . Woodhead, Cambridge 2007, ISBN 978-1-84569-175-2 .
- Thorsten Proettel: Das Wichtigste über Goldanlagen, Ratgeber Vermögensanlage . Sparkassen Verlag, Stuttgart 2012.
- Hans-Jochen Schneider: Gold in Amerika. In: Die Geowissenschaften. Bd. 10, Nr. 12, 1992, S. 346–352. doi:10.2312/geowissenschaften.1992.10.346 .
- Christoph J. Raub, Esther P. Wipfler: Gold (Werkstoff) . In: RDK . Labor (2014).
- Bernd Stefan Grewe: Gold. Eine Weltgeschichte (= CH Beck Wissen. Bd. 2889). CH Beck, München 2019, ISBN 978-3-406-73212-6 .
Weblinks
- Material Archiv: Feingold – Umfangreiche Materialinformationen und Bilder
- Mineralienatlas:Gold – Gold als Mineral
- Woher kommt unser Gold? aus der Fernseh-Sendereihe alpha-Centauri (ca. 15 Minuten). Erstmals ausgestrahlt am 3. Dez. 2000.
Einzelnachweise
- ↑ a b David R. Lide (Hrsg.): CRC Handbook of Chemistry and Physics . 90. Auflage. (Internet-Version: 2010), CRC Press/Taylor and Francis, Boca Raton, FL, Geophysics, Astronomy, and Acoustics; Abundance of Elements in the Earth's Crust and in the Sea, S. 14-18.
- ↑ Die Werte für die Eigenschaften (Infobox) sind, wenn nicht anders angegeben, aus www.webelements.com (Gold) entnommen.
- ↑ IUPAC Commission on Isotopic Abundances and Atomic Weights: Standard Atomic Weights of 14 Chemical Elements Revised. In: Chemistry International. 40, 2018, S. 23, doi : 10.1515/ci-2018-0409 .
- ↑ a b c d e Eintrag zu gold in Kramida, A., Ralchenko, Yu., Reader, J. und NIST ASD Team (2019): NIST Atomic Spectra Database (ver. 5.7.1) . Hrsg.: NIST , Gaithersburg, MD. doi : 10.18434/T4W30F ( https://physics.nist.gov/asd ). Abgerufen am 13. Juni 2020.
- ↑ a b c d e Eintrag zu gold bei WebElements, https://www.webelements.com , abgerufen am 13. Juni 2020.
- ↑ NN Greenwood, A. Earnshaw: Chemie der Elemente. 1. Auflage. VCH, Weinheim 1988, ISBN 3-527-26169-9 , S. 1509.
- ↑ a b c Gold . In: John W. Anthony, Richard A. Bideaux, Kenneth W. Bladh, Monte C. Nichols (Hrsg.): Handbook of Mineralogy, Mineralogical Society of America . 2001 ( handbookofmineralogy.org [PDF; 57 kB ; abgerufen am 11. Januar 2018]).
- ↑ Robert C. Weast (Hrsg.): CRC Handbook of Chemistry and Physics. CRC (Chemical Rubber Publishing Company), Boca Raton 1990, ISBN 0-8493-0470-9 , S. E-129 bis E-145. Werte dort sind auf g/mol bezogen und in cgs-Einheiten angegeben. Der hier angegebene Wert ist der daraus berechnete maßeinheitslose SI-Wert.
- ↑ a b Yiming Zhang, Julian RG Evans, Shoufeng Yang: Corrected Values for Boiling Points and Enthalpies of Vaporization of Elements in Handbooks. In: Journal of Chemical & Engineering Data . Bd. 56, 2011, S. 328–337, doi:10.1021/je1011086 .
- ↑ Ludwig Bergmann, Clemens Schaefer, Rainer Kassing: Lehrbuch der Experimentalphysik . Band 6: Festkörper. 2. Auflage. Walter de Gruyter, 2005, ISBN 3-11-017485-5 , S. 361.
- ↑ a b Eintrag zu Gold in der GESTIS-Stoffdatenbank des IFA , abgerufen am 25. April 2017. (JavaScript erforderlich)
- ↑ Kluge. Etymologisches Wörterbuch der deutschen Sprache . Bearbeitet von Elmar Seebold . 25., durchgesehene und erweiterte Auflage. De Gruyter, Berlin/Boston 2011, S. 366.
- ↑ Tom Higham ua: New perspectives on the Varna cemetery (Bulgaria) – AMS dates and social implications . In: Antiquity Journal . Band 81 , Nr. 313 . New York 2007, S. 640–654 .
- ↑ Svend Hansen: Gold und Silber in der Maikop-Kultur. In: Metalle der Macht – Frühes Gold und Silber. Abstracts des 6. Mitteldeutschen Archäologentages, 17. bis 19. Oktober 2013. (PDF) .
- ↑ Silke Schwarzländer: Ältestes Gold Brandenburgs. Reiche Sonderbestattung der Glockenbecherkultur in Wustermark, Lkr. Havelland. In: Archäologie in Berlin und Brandenburg . Band 2004 . Konrad Theiss Verlag, Darmstadt 2005, S. 34–35 .
- ↑ Neolithisches Gold: Exzeptioneller Befund beim Brückenbau in Wustermark, Lkr. Havelland. (Nicht mehr online verfügbar.) Brandenburgisches Landesamt für Denkmalpflege, archiviert vom Original am 16. August 2014 ; abgerufen am 2. Dezember 2014 .
- ↑ Alfred Grimm , Sylvia Schoske : Das Geheimnis des goldenen Sarges: Echnaton und das Ende der Amarnazeit. München 2001.
- ↑ Wilhelm Hassenstein, Hermann Virl : Das Feuerwerkbuch von 1420. 600 Jahre deutsche Pulverwaffen und Büchsenmeisterei. Neudruck des Erstdruckes aus dem Jahr 1529 mit Übertragung ins Hochdeutsche und Erläuterungen von Wilhelm Hassenstein. Verlag der Deutschen Technik, München 1941, S. 102 f.
- ↑ United States Geological Survey: World Mine Production and Reserves January 2017
- ↑ Goldsuche extrem: Südafrikaner wollen 5000 Meter runter. auf: goldreporter.de , 18. Februar 2011.
- ↑ MinEx Consulting: Long term trends in gold exploration , S. 18.
- ↑ Fundortliste für gediegen Gold beim Mineralienatlas und bei Mindat
- ↑ Matthias Oppliger: Ein Riesenknall und dann sind da Welten aus Gold. In: TagesWoche. 24. Dezember 2017. (tageswoche.ch)
- ↑ https://www.geographie.uni-wuerzburg.de/fileadmin/04140600/WR_BKGR/Frimmel_Wits_SEG_SP18_2014.pdf
- ↑ WEL Minter, M. Goedhart, J. Knight, HE Frimmel: Morphology of Witwatersrand gold grains from the Basal Reef; evidence for their detrital origin. In: Economic Geology. Band 88, Nr. 2, April 1993, S. 237–248doi:10.2113/gsecongeo.88.2.237 .
- ↑ Hartwig E. Frimmel, WE Lawrie Minter, John Chesley, Jason Kirk, Joaquin Ruiz: Short-range gold mobilisation in palaeoplacer deposits. In: Mineral Deposit Research: Meeting the Global Challenge. 2005, S. 953–956, doi : 10.1007/3-540-27946-6_243 .
- ↑ HE Frimmel: Earth's continental crustal gold endowment: Earth Planet. In: Sci. Letters. Bd. 267, 2008, S. 45–55.
- ↑ RH Sillitoe, JW Hedenquist Linkages between volcanotectonic settings, ore-fluid compositions, and epithermal precious-metal deposits . In: Society of Economic Geologists Special Publication 10, 315–343, 2003
- ↑ Holcim Kies und Beton GmbH erwirbt neue Kieswerke und ein Trockensandwerk. ( Memento vom 28. Juni 2012 im Internet Archive ) Pressemitteilung Holcim-Süd. 1. April 2008, abgerufen am 23. August 2012.
- ↑ Christoph Seidler: Schatzsucher heben das Rheingold. In: Spiegel Online. 23. August 2012. abgerufen am gleichen Tage.
- ↑ US Geological Survey, Gold Statistics and Information , Zugriff am 26. Oktober 2012.
- ↑ a b Thomas Jüstel: Chemie Rekorde (PDF-Datei). Abgerufen im Juni 2020
- ↑ Infografik: Goldbarren .
- ↑ Euromax Ressources: Technical Report on the Gold Resources at Trun Property – Trun and Breznik Municipalities, Pernik District, Bulgaria. ( Memento vom 10. April 2014 im Internet Archive ) (PDF; 5,7 MB).
- ↑ Northland: Barsele Rapidly-Growing Gold Resource. ( Memento vom 14. Februar 2009 im Internet Archive ) (englisch).
- ↑ IMA/CNMNC List of Mineral Names; September 2017 (PDF 1,67 MB; Gold siehe S. 76)
- ↑ IMA/CNMNC List of Mineral Names; 2009 (PDF 1,8 MB, Gold siehe S. 109).
- ↑ Webmineral – Minerals Arranged by the New Dana Classification. 01.01.01 Gold group .
- ↑ Webmineral – Mineral Species sorted by the element Au (Gold)
- ↑ Edelmetalle – Gold ( Memento vom 9. April 2011 im Internet Archive ) (PDF; 197,1 kB, S. 4).
- ↑ Größter Goldfund aller Zeiten. In: Hielscher oder Haase. Deutschlandfunk Nova, 12. September 2018, abgerufen am 27. April 2020 .
- ↑ Shannon Venable: Gold: A Cultural Encyclopedia. ABC-CLIO, 2011, ISBN 978-0-313-38431-8 , S. 118.
- ↑ Illegale Schürfer: Teures Gold zerstört den Regenwald. In: Spiegel online. 20. April 2011.
- ↑ Justus Freiherr von Liebig , Johann Christian Poggendorff , Friedrich Wöhler (Hrsg.): Handwörterbuch der reinen und angewandten Chemie . Friedrich Vieweg und Sohn, Braunschweig 1842 ( eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ Siehe das Gold-Quecksilber-Phasendiagramm bei: H. Okamoto, TB Massalski: The Au-Hg (Gold Mercury) System. In: Bulletin of Alloy Phase Diagrams. 1989, doi:10.1007/BF02882176 .
- ↑ Chemicals and Waste Branch UNEP: ASGM: Eliminating the worst practices . YouTube, September 2017.
- ↑ gold extraction ( Memento vom 16. August 2013 im Internet Archive ), englisch, bei geology.com
- ↑ Peter WU Appel, Leoncio Na-Oy: The Borax Method of Gold Extraction for Small-Scale Miners . In: Journal of Health and Pollution . Band 2 , Nr. 3 , 2012 ( journalhealthpollution.org [PDF; abgerufen am 2. Dezember 2014]).
- ↑ John O. Marsden, C. Iain House: The Chemistry of Gold Extraction. 2. Auflage. Society for Mining, Metallurgy and Exploration, 2006, ISBN 0-87335-240-8 , S. 455. (teilweise einsehbar bei Google-Books) .
- ↑ Borax replacing mercury in small-scale mining PDF-Datei ( Memento vom 18. Februar 2015 im Internet Archive ).
- ↑ Walter A. Franke: Quick assays in mineral identification A guide to experiments for mineral collectors and geoscientists in field work. ( PDF-Datei , englisch).
- ↑ Siehe die Videos bei Mercury-free gold mining ; bei appelglobal.com.
- ↑ a b Filipino Gold Miner's Borax Revolution ( Memento vom 13. Oktober 2016 im Internet Archive ), Website des Blacksmith Institute , März/April 2012.
- ↑ John O. Marsden, C. Iain House: The Chemistry of Gold Extraction. 2. Auflage. Society for Mining, Metallurgy and Exploration, 2006, ISBN 0-87335-240-8 , S. 457.
- ↑ World Gold Council: Gold Demand Trends
- ↑ Jan Dönges: Klärschlamm enthält Gold für Millionen von Euro. In: Spektrum der Wissenschaft online. 20. Januar 2015, abgerufen am 5. November 2016 .
- ↑ Güsel ist Gold wert – Die KEZO ist das «Mekka des Schweizer Metallrecycling». In: srf.ch . 30. Januar 2018, abgerufen am 1. Februar 2018.
- ↑ Krematorien beraten über Zahngold. ORF.at, 4. September 2013.
- ↑ Ralf Hahn: Gold aus dem Meer. Die Forschungen des Nobelpreisträgers Fritz Haber in den Jahren 1922–1927. 1999.
- ↑ Dietrich Stoltzenberg: Gold aus dern Meer? – Fritz Habers Arbeiten über den Goldgehalt im Meerwasser. In: Chemie in unserer Zeit . Bd. 28, Nr. 6, 1994, S. 321–327, doi:10.1002/ciuz.19940280611
- ↑ Reinhard Osteroth: Wirtschaftsgeschichte: Geld in Not? Gold aus dem Meer! In: Die Zeit . Nr. 35/2011 ( online ).
- ↑ K. Kenison Falkner, J. Edmond: Gold in seawater. In: Earth and Planetary Science Letters. Bd. 98, Nr. 2, 1990, S. 208–221, doi:10.1016/0012-821X(90)90060-B .
- ↑ Ernst von Meyer : Geschichte der Chemie . 1914.
- ↑ Lotte Kurras: Nikolaus von Paris. In: Verfasserlexikon . Band VI, Sp. 1128.
- ↑ Gefährlicher Goldabbau: „Ein Ehering produziert 20 Tonnen Giftmüll“. In: Spiegel online. 20. März 2008. (spiegel.de)
- ↑ Minería Aurífera en Madre de Dios y contaminación con Mercurio. (PDF; 10,0 MB) (Nicht mehr online verfügbar.) In: Umweltministerium Peru. 2011, archiviert vom Original am 9. Mai 2012 ; abgerufen am 26. August 2012 (spanisch).
- ↑ Gefährliches Quecksilber beim Goldwaschen. auf: derstandard.at , 5. März 2009.
- ↑ Goldförderung bedroht Mensch und Umwelt. Rettet den Regenwald , 19. März 2008.
- ↑ Öko-Gold: Englische Goldbarren erhalten erstmals Umwelt-Label. Goldreporter
- ↑ Ralph WG Wyckoff: Crystal Structures . 2. Auflage. Band 1 . John Wiley & Sons, New York/ London, Sydney 1963, S. 3 (im Anhang ).
- ↑ Hugo Strunz , Ernest H. Nickel : Strunz Mineralogical Tables. Chemical-structural Mineral Classification System . 9. Auflage. E. Schweizerbart'sche Verlagsbuchhandlung (Nägele u. Obermiller), Stuttgart 2001, ISBN 3-510-65188-X , S. 34 .
- ↑ Neue Struktur des Goldes entdeckt. Abrupte Kompression macht Atomgitter des Goldes erst locker, dann sogar flüssig. In: scinexx.de. scinexx das wissensmagazin, 5. August 2019, abgerufen am 27. September 2019 .
- ↑ Friedrich Klockmann : Klockmanns Lehrbuch der Mineralogie . Hrsg.: Paul Ramdohr , Hugo Strunz . 16. Auflage. Enke, Stuttgart 1978, ISBN 3-432-82986-8 , S. 395 (Erstausgabe: 1891).
- ↑ Porpezite , Mindat.
- ↑ Physik Journal. Februar 2017, S. 19.
- ↑ Relativity in Chemistry. Math.ucr.edu, abgerufen am 5. April 2009 .
- ↑ Hubert Schmidbaur, Stephanie Cronje, Bratislav Djordjevic, Oliver Schuster: Understanding gold chemistry through relativity . In: Chemical Physics . Band 311 , Nr. 1–2 , 2005, S. 151–161 , doi : 10.1016/j.chemphys.2004.09.023 , bibcode : 2005CP....311..151S .
- ↑ Chemie: Risse im Periodensystem. In: spektrum.de. Abgerufen am 19. Januar 2019 .
- ↑ JV Barth, H. Brune, G. Ertl, RJ Behm: Scanning tunneling microscopy observations on the reconstructed Au(111) surface: Atomic structure, long-range superstructure, rotational domains, and surface defects. In: Phys. Rev. B . Bd. 42, 1990, S. 9307–9318, doi:10.1103/PhysRevB.42.9307 .
- ↑ Gesetzliche Begrenzung von Abwasseremissionen aus der Herstellung und Weiterverarbeitung von Edelmetallen und der Herstellung von Quecksilbermetall, bei lebensministerium.at, (PDF-Datei) ( Memento vom 7. März 2014 im Internet Archive ), S. 4.
- ↑ Arnold Holleman, Egon Wiberg: Lehrbuch der Anorganischen Chemie. 91.–100., verb. und stark erw. Auflage. Walter de Gruyter, Berlin/ New York 1985, ISBN 3-11-007511-3 .
- ↑ Ätzen von Gold mit KI/I 2
- ↑ Yongfeng Zhu, Fang An, Juanjuan Tan: Geochemistry of hydrothermal gold deposits: A review. In: Geoscience Frontiers. 2, 2011, S. 367, doi:10.1016/j.gsf.2011.05.006 .
- ↑ Brian J. Alloway: Schwermetalle in Böden, Analytik, Konzentration, Wechselwirkungen Springer-Verlag, 1999, ISBN 3-642-63566-0 , S. 341, doi:10.1007/978-3-642-58384-1 .
- ↑ Gold demand gold.org (englisch). Zu den Prozentangaben siehe die Unterabschnitte Jewellery, Investment, Central Banks, Technology .
- ↑ Gold demand: Jewellery gold.org (englisch)
- ↑ Eintrag zu E 175: Gold in der Europäischen Datenbank für Lebensmittelzusatzstoffe, abgerufen am 16. Juni 2020.
- ↑ World Gold Council: World Official Gold Holdings, Dezember 2011.
- ↑ Thorsten Proettel: Das Wichtigste über Goldanlagen, Ratgeber Vermögensanlage. Sparkassen Verlag, Stuttgart 2012.
- ↑ Thorsten Proettel: Das Wichtigste über Goldanlagen, Ratgeber Vermögensanlage. Sparkassen Verlag, Stuttgart 2012, S. 7 und 24.
- ↑ Leiterplatten-Oberflächen , abgerufen im September 2015.
- ↑ Wolfgang Miehle: Gelenk- und Wirbelsäulenrheuma. Eular Verlag, Basel 1987, ISBN 3-7177-0133-9 , S. 77 f.
- ↑ Auskunft zur Marke Herzgold im Register des Deutschen Patent- und Markenamtes (DPMA)
- ↑ CJS Thompson: The dawn of medicine. A chapter in the history of pharmacy from the earliest times to the tenth century. In: Janus. Bd. 28, 1924, S. 425–450, hier: S. 448.
- ↑ Gundolf Keil: „blutken – bloedekijn“. Anmerkungen zur Ätiologie der Hyposphagma-Genese im ‚Pommersfelder schlesischen Augenbüchlein' (1. Drittel des 15. Jahrhunderts). Mit einer Übersicht über die augenheilkundlichen Texte des deutschen Mittelalters. In: Fachprosaforschung – Grenzüberschreitungen. Bd. 8/9, 2012/2013, S. 7–175, hier: S. 18, 21 und 43.
- ↑ Paul Diepgen : Gualtari Agilonis Summa medicinalis. Nach den Münchner Cod. la. Nr. 325 und 13124 erstmalig ediert mit einer vergleichenden Betrachtung älterer medizinischer Kompendien des Mittelalters. Leipzig 1911, S. 72 (pillul[a]e aure[a]e) .
- ↑ W. Heuck: Die Goldtherapie, eine notwendige Ergänzung der bisherigen Syphilis-Therapie, Verhandlungen der deutschen Dermatologischen Gesellschaft 17. Kongress gehalten zu Berlin 8.–10. Oktober 1935. In: Arch. Dermatol. Syph. Bd. 172, 1935, S. 75–79.
- ↑ TE Durkes: Gold bead implants . In: Probl Vet Med . Nr. 4 , 1992, S. 207–211 , PMID 1581658 .
- ↑ A. Larsen, M. Stoltenberg, G. Danscher: In vitro liberation of charged gold atoms: autometallographic tracing of gold ions released by macrophages grown on metallic gold surfaces . In: Histochem Cell Biol . Band 128 , 2007, S. 1–6 , PMID 17549510 .
- ↑ Datei:Image-Metal-reflectance.png , M. Bass,EW Van Stryland (Hrsg.): Handbook of Optics. 2. Auflage. vol. 2, McGraw-Hill, 1994, ISBN 0-07-047974-7 .
- ↑ C. Couto, R. Vitorino, AL Daniel-da-Silva: Gold nanoparticles and bioconjugation: a pathway for proteomic applications. In: Critical reviews in biotechnology. [elektronische Veröffentlichung vor dem Druck] Februar 2016, doi:10.3109/07388551.2016.1141392 . PMID 26863269 .
- ↑ Pablo D. Jadzinsky, Guillermo Calero1, Christopher J. Ackerson, David A. Bushnell, Roger D. Kornberg: Structure of a Thiol Monolayer-Protected Gold Nanoparticle at 1.1 Å Resolution. In: Science. Bd. 318, 2007, S. 430–433; doi:10.1126/science.1148624 .
- ↑ Cyrille Gautier, Thomas Bürgi: Chiral Inversion of Gold Nanoparticles. In: J. Am. Chem. Soc. Bd. 130, 2008, S. 7077–7084, doi:10.1021/ja800256r .
- ↑ Jochem Wolters: Der Gold- und Silberschmied. Band 1: Werkstoffe und Materialien. 2., durchgesehene Auflage. Rühle-Diebener-Verlag, Stuttgart 1984, Kapitel 1.4.8 Kupfer und seine Legierungen .
- ↑ Gold auf Echtheit prüfen: So fliegt jeder Schwindel auf. Abgerufen am 3. Mai 2021 .
- ↑ Eintrag zu magnetische Waage. In: Römpp Online . Georg Thieme Verlag, abgerufen am 3. Mai 2021.
- ↑ Georg Brauer (Hrsg.), unter Mitarbeit von Marianne Baudler ua: Handbuch der Präparativen Anorganischen Chemie. 3., umgearbeitete Auflage. Band II, Ferdinand Enke, Stuttgart 1978, ISBN 3-432-87813-3 .
- ↑ MS Wickleder: AuSO 4 , a true gold(II) sulfate with an Au 2 4+ cation. In: Z. Anorg. Allg. Chem. Bd. 627, 2001, S. 2112–2114 doi : 10.1002/1521-3749(200109)627:9<2112::AID-ZAAC2112>3.0.CO;2-2
- ↑ Alles zur Allergologie – Gold .
- ↑ Blutgold aus dem Kongo. In: Spiegel online. abgerufen am 8. Januar 2014.
- ATC-V10
- Gruppe-11-Element
- Übergangsmetall
- Schwermetall
- Periode-6-Element
- Chemisches Element
- Wikipedia:Lesenswert
- Gold
- Grandfathered Mineral
- Kubisches Kristallsystem
- Elemente (Mineralklasse)
- Lebensmittelfarbstoff
- Elektrotechnischer Werkstoff
- Zahlungsmittel
- Lebensmittelzusatzstoff (EU)



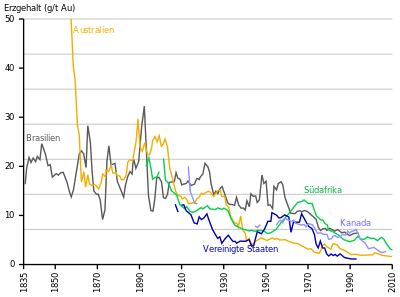













![{\displaystyle {\ce {2Au + H2O + 1/2O2 + 4NaCN -> 2Na[Au(CN)2] + 2NaOH}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/ec157dd1cfa23c50e477edc56b74f5f771451567)
![{\displaystyle {\ce {2Na[Au(CN)2] + Zn -> Na2[Zn(CN)4] + 2Au}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/257e589e015d6284d6274da0158a55d09e72feb5)










![{\displaystyle {\ce {2Au + 1/2O2 + H2O + 4KCN -> 2K[Au(CN)2] + 2KOH}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/11d7d454b710143af9dc08cd8c6dc29c9228c90b)
![{\displaystyle {\ce {2Au + 4{Thioharnstoff (TH)}+ Fe2(SO4)3 -> [Au(TH)2]2SO4 + 2FeSO4}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/338f74a7d8f48e73ced0f7cd3c42f55602e55b42)