vann
Vann (H2O) er en kjemisk forbindelse som består av elementene oksygen (O) og hydrogen (H). Begrepet vann brukes om den flytende aggregeringstilstanden . I fast tilstand snakker man om is , i gassform av vanndamp . I naturen forekommer vann sjelden i ren form, men inneholder for det meste oppløste komponenter av salter, gasser og organiske forbindelser.
Vann muliggjør liv på jorden . Den har en enestående kulturell betydning i alle sivilisasjoner og regnes for å være en av de mest vitenskapelig godt studerte kjemiske forbindelsene . Siden vann er det eneste naturlige stoffet på jorden som forekommer i fast, flytende og gassform , former det livløs natur fra geologiske prosesser innen millioner av år til værfenomener hvert minutt. Biologiske prosesser finner bare sted takket være vann, og mennesker som biologiske vesener bruker vann for å sikre sin egen overlevelse og for deres kulturelle og økonomiske utvikling. Det er derfor åpenbart at vann har fått religiøs betydning for mange sivilisasjoner.
Betegnelser
etymologi
Ordet “vann” er avledet fra det gamle Høy tyske waȥȥar, “fuktig, flyter”. [1] De indoeuropeiske navnene * wódr̥ og * wédōr er allerede i hettittiske tekster fra det andre årtusen f.Kr. Okkupert. Beslektede ord kan også finnes på andre indoeuropeiske språk, f.eks. B.
- Germansk: tysk vann ; engl. vann ; isl. vatn
- Celtic: schott. Uisge (jf. Whisky ); ir. uisce
- Slavisk: russisk вода ( voda , jf. Vodka ); stang. voda ; øvre sorb. voda
- Baltikum: lit. vanduo ; lett. ūdens
Det gamle greske ordet ὕδωρ, hydor , "vann", som alle fremmede ord med ordet komponent hydr (o) - er avledet fra, tilhører denne familien.
Den arabiske roten "DRR" med betydningen "å flyte" er lik.
Alternative kjemiske navn
Andre navn på vann - tillatt i henhold til den kjemiske nomenklaturen - er:
- Hydrogen oksyd: Det finnes imidlertid også andre oksyder av hydrogen (se hydrogen oksyder ).
- Diwasserstoffmonoxid, Wasserstoffhydroxid, Dihydrogeniumoxid, Hydrogeniumoxid, Hydrogeniumhydroxid, oxane, Oxidan ( IUPAC ) eller Dihydrogen (DHMO).
Egenskaper for vann
med alle kjemiske og fysiske data i infoboksen , bruk som en kjemisk og tetthetsanomali i vannet .
Vann (H2O) er en kjemisk forbindelse som består av elementene oksygen (O) og hydrogen (H). Som væske er vann gjennomsiktig, stort sett fargeløst, luktfritt og smakløst. Det forekommer i to isomerer (para og ortho vann), som er forskjellige i atomspinnet til de to hydrogenatomer.
Vannmolekyl
Vann består av molekyler , som hver består av to hydrogenatomer og ett oksygenatom .
På Pauling -skalaen har oksygen en høyere elektronegativitet med 3,5 enn hydrogen med 2,1. Som et resultat har vannmolekylet uttalte delvise ladninger , med en negativ polaritet på siden av oksygenet og en positiv polaritet på siden av de to hydrogenatomer. Resultatet er en dipol hvis dipolmoment i gassfasen er 1,84 Debye .
Hvis vann forekommer som en ligand i en kompleks binding, er vann en monodentatligand .
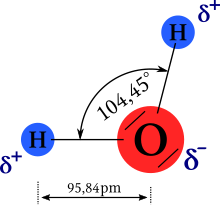
Vannmolekylet er geometrisk vinklet, med de to hydrogenatomer og de to elektronparene som peker inn i hjørnene av et tenkt tetraeder . Vinkelen som omsluttes av de to OH -bindingene er 104,45 °. Den avviker fra den ideelle tetraedervinkelen (~ 109,47 °) på grunn av den økte plassen som kreves av de ensomme elektronparene. Bindingslengden til OH -bindingene er 95,84 pm i hvert tilfelle.
På grunn av kjernespinnet til hydrogenatomer forekommer vannmolekyler i to isomerer ( para og ortho vann ) med nesten identiske fysiske egenskaper. Det er mulig å skille de to formene og studere de forskjellige kjemiske reaktivitetene. [2] [3]
Fordi vannmolekyler er dipoler , har de uttalte intermolekylære tiltrekningskrefter og kan samles i klynger gjennom hydrogenbindinger . Dette er ikke faste, faste kjeder. Tilkoblingen via hydrogenbindinger varer bare i en brøkdel av et sekund, hvoretter de enkelte molekylene løsner seg fra forbindelsen og kobler seg på nytt med andre vannmolekyler på like kort tid. Denne prosessen gjentar seg kontinuerlig og fører til slutt til dannelsen av variable klynger. Disse prosessene forårsaker de spesielle egenskapene til vann:
Har vann
- en tetthet på rundt 1000 kg / m³ (opprinnelig definisjonen av kilogrammet), nærmere bestemt: 999,975 kg / m³ ved 3,98 ° C. Tetthetsanomalien er egenskapen basert på hydrogenbindingen at vann har den høyeste tettheten ved denne temperaturen og øker i volum kontinuerlig når det avkjøles under denne temperaturen og til og med brått når det fryser, dvs. det mister tetthet slik at is flyter på vann,
- en viskositet på 1,0019 mPas (0,010019 poise ) ved 20 ° C [4] ,
- en av de høyeste spesifikke varmekapasitetene til væsker ved romtemperatur (75,366 J mol −1 K −1 tilsvarende 4,18 kJ kg −1 K −1 ved 20 ° C [5] ),
- en av de største overflatespenningene for alle væsker ( kvikksølv har imidlertid en enda større); med vann er det 72 mN / m i fuktig luft ved +20 ° C, slik at dråpedannelsen blir lettere,
- en av de største spesifikke fordampningsenthalpiene til alle væsker (44,2 kJ / mol tilsvarende 2453 kJ / kg ved 20 ° C; derav kjøleeffekten under transpirasjon ) og en høysmeltende entalpi (6,01 kJ / mol som tilsvarer 333 kJ / kg; slik at saltvann bare viser en liten depresjon av frysepunktet sammenlignet med rent vann),
- lav varmeledningsevne (0,6 W / (m K) ved 20 ° C).
Avhengig av den isotopiske sammensetning av vannmolekylet til normal "lett vann" er forskjellig (to atomer av hydrogen : H 2 O), " Medium Heavy vann " (et atomært hydrogen og atom deuterium : HDO), " tungtvann " (to atomer av deuterium: D 2 O) og “ supertungt vann ” (to atomer av tritium : T 2 O), med HTO og DTO også forekommende med andre molekyler med blandede isotoper.
Under høyspenning kan vann danne en vannbro mellom to glassbeholdere. [6]
Syntese, elektrolyse og kjemisk bruk
Vann som kjemisk forbindelse ble først syntetisert da Henry Cavendish eksploderte en blanding av hydrogen og luft på 1700 -tallet (se oksyhydrogenreaksjon ).
Hydrogen regnes som fremtidens energibærer . [7]
I likhet med elektrisk energi er hydrogen ikke en primærenergi, men må produseres fra primærenergi, analogt med elektrisitetsproduksjon .
For demonstrasjonen brytes vann ned i komponentene i Hofmanns vannnedbrytingsapparat . Reaksjonsskjema :
bevis
Deteksjonsreaksjon : vann blir hvitt kobbersulfat , fritt for krystalliseringsvann, lyseblått og blått kobolt (II) kloridpapir farges rødt av vann.
I analyse er vann i små mengder ( fuktighet eller tørrhet ) hovedsakelig kvantifisert ved hjelp av Karl Fischer -titrering (ifølge Karl Fischer ). Monografier i farmakopéer for kvantitativ påvisning av vann er hovedsakelig basert på Karl Fischer -titrering.
Dannelse av boblene i kokende vann
Eksponering for varme får vannmolekylene til å bevege seg raskere. Hvis 100 ° C er nådd på det punktet hvor varmen påføres, skifter den (avhengig av kimen med mer eller mindre forsinket koking ) fra væsken til den gassformige aggregeringstilstanden (damp), hvis volum er rundt 1600 ganger høyere (se vanndamp ) og som på grunn av sin lavere tetthet i forhold til vannet rundt stiger som mer eller mindre store bobler: Vannet begynner å koke , hvorved dampen bobler fra lag med vann som ennå ikke er så varme blir avkjølt og kondenserer tilbake til flytende vann. Når hele vannmengden endelig når en temperatur på 100 ° C, når de nå store dampboblene overflaten: vannet koker.
Trykk og temperatur er avgjørende faktorer for løseligheten av gasser i vann. Gassbobler som blir synlige selv ved litt oppvarming, består ikke av vanndamp, men av oppløste gasser. Årsaken er den lavere vannløseligheten til gasser ved oppvarming. Vann igjen i et rør eller en flaske under trykk en stund har ofte løst opp overflødige gasser. Derfor er det bare å fjerne det ytre trykket nok til at gassbobler skilles ut - helst på bakterier på veggen - og holder seg til dem opp til en størrelse på 1-2 mm.
Vann og mann
Historien om vannbruk
Historien om menneskelig bruk av vann, og dermed hydrologi , vannforvaltning og spesielt hydraulikk , er preget av et relativt lite antall grunnleggende motiver. Fra de første bosatte menneskene til de avanserte kulturene i antikken gjennom middelalderen til moderne tid, har fokus alltid vært på en konflikt mellom for mye og for lite vann. Du var nesten alltid prisgitt ham, enten høsten kom på grunn av tørke eller flom truet liv og eiendom. Det ble også gjenstand for mytologi og naturfilosofi . Selv i dag har vann en spesiell posisjon i de fleste av verdens religioner, spesielt der spørsmålet om overlevelse avhenger av løsningen på de mange vannproblemene.
Målet var å oppfylle alle brukskrav og å garantere alle den delen av vannet de har krav på. Vannloven fungerte som en av de første juridiske formene for å grunnlegge de første sentraliserte sivilisasjonene i Mesopotamia og Egypt, så vel som de som dukket opp i elvedalene i Kina og India.
Den lange historien til vannbruk, som menneskets historie som helhet, viser seg ikke som en kontinuerlig utviklingsvei. Det ble hovedsakelig preget av individuelle sentre med høye vannforvaltningsstandarder og av tilbakevendende pauser, i tillegg til faser av stagnasjon som ofte varte i århundrer. Så imponerende som de tidlige hydrauliske konstruksjonene var, hvor stor innovasjonsstyrken og kreativiteten til våre forfedre var, til syvende og sist var man og er fortsatt avhengig av naturen, som man først har begynt å forstå relativt nylig.
Vann i gammel vitenskap og filosofi
På grunn av vannets store betydning, var det ikke tilfeldig at de tidligste filosofene regnet det blant de fire urelementene . Thales of Miletus så til og med det primære stoffet av alt å være i vann. I teorien med fire elementer som ble introdusert av Empedokles og deretter hovedsakelig representert av Aristoteles , er vann et element ved siden av ild , luft og jord .
Vann er representert i den taoistiske femelementsundervisningen (ved siden av tre, ild, jord og metall ). Imidlertid er begrepet elementer litt misvisende her, siden dette er forskjellige endringsfaser i en syklisk prosess. Vann har forskjellige retninger som fører til forskjellige (symbolske) strukturer. [Åttende]
I det gamle Hellas ble icosahedron tildelt elementet vann som et av de fem platoniske faste stoffene .
Vann i religion
Vann er sentralt i mytologiene og religionene i de fleste kulturer. Med før-sosratikken, for rundt 2500 år siden, begynte vestlig tenkning som en filosofi om vann. I mange gamle religioner ble vannet generelt og kilder spesielt æret som helligdommer. [9] De ufødte barna ble antatt å være gjemt i kilder, brønner eller dammer, som barnepigene ( jordmødrene ) hentet dem fra (barns tro).
Vann er livets symbol. Det har høy prioritet i religionene. Vannets rensekraft påkalles ofte, for eksempel i islam i form av den rituelle ablusjonen før man går inn i en moské, eller i hinduistisk tro under et rituelt bad i Ganges .
Nesten alle samfunn i jødedommen har en mikveh , et rituelt bad med rennende rent vann som ofte kommer fra en dyp grunnvannsbrønn når kildevann ikke er tilgjengelig. Bare de som er helt nedsenket, blir rituelt renset. Dette er nødvendig for konvertitter til jødedommen, for kvinner etter menstruasjon eller fødsel og for ortodokse jøder før sabbaten og andre høytider.
I kristendommen utføres dåpen delvis ved nedsenking eller dousing med vann som en helkroppsdåp , i den vestlige kirken i dag for det meste ved å dusje med vann. I den katolske kirke, de ortodokse kirker og den anglikanske kirken spiller velsignelsen med hellig vann en spesiell rolle.
Vann i esoterismen
I esoterismen spiller vann en rolle, maktsteder søkes ofte ved kilder eller elver.
Vann i tekst
Mange dikt omhandler vann og er oppsummert i antologier . [10]
Vann i sagn og bevingede ord
Vann spiller en rolle i mange sagn og eventyr , for eksempel i Das Wasser des Lebens av brødrene Grimm. Betydningen av vann kan bli funnet i det bevingede ordet No water can cloud .
Menneskelig helse
Menneskekroppen består av over 70% vann. Mangel på vann fører derfor til alvorlige helseproblemer hos mennesker ( dehydrering , uttørking ), ettersom kroppens funksjoner som er avhengige av vann er begrenset. Sitat fra German Nutrition Society (DGE) : Hvis dette (vannforsyningen) er utilstrekkelig, kan det føre til svimmelhet, sirkulasjonsforstyrrelser, oppkast og muskelkramper, siden tilførsel av oksygen og næringsstoffer til muskelcellene er begrenset når vann er tapt. [11]
Hvor høyt det daglige minstekravet er, er uklart. Anbefalinger på 1,5 liter og mer per dag for en frisk voksen kan ikke støttes vitenskapelig. [12] Med et gjennomsnittlig daglig forbruk på 2 liter vil det bli drukket over 55 000 liter vann på 80 år. Vannbehovet kan være større ved høyere temperaturer.
Å drikke for store mengder vann med mer enn 20 L / dag kan også føre til helseproblemer. " Vannforgiftning " kan oppstå eller, mer presist, føre til mangel på salter, dvs. til hyponatremi med permanent nevrologisk skade eller død.[1. 3]
I medisin brukes vann (i form av isotoniske løsninger) hovedsakelig til infusjoner og injeksjoner . Ved innånding brukes for eksempel aerosolisert vann for å helbrede hoste.
Vann, påført eksternt, har svært gunstige effekter på helse og hygiene. Se også : bading , balneologi , Kneippterapi , badstue , svømming , vask . Av disse grunnene dyrket de gamle romerne en "vannkultur" i termalbadene.
Viktighet for dyrking, økonomi og utvikling
Vann er et grunnleggende krav for livet: uten regn er det ingen drikkevannstilførsel, ingen jordbruk, ingen vannmasser med fisk til forbruk, ingen elver for transport av varer, ingen industri. Sistnevnte krever mye vann for alle produksjonsprosesser, som blir avklart og returnert til syklusen. På grunn av den høye fordampningsvarmen i form av damp, brukes vann til å drive dampmotorer og dampturbiner og til å varme kjemiske produksjonsanlegg. På grunn av sin høye varmekapasitet og fordampningsvarme, fungerer vann som et sirkulerende eller fordampende kjølevæske; I 1991 alene i Tyskland ble 29 milliarder m³ brukt som kjølevann i kraftverk. Vann kan også brukes som kjølemiddel (R-718) i kjølemaskiner. [14] I saltgruvedrift brukes vann som løsningsmiddel for utvasking, transport, saltlake og rengjøring.
Vann som drikkevann, produkt og vare
Vannforsyningen bruker forskjellige vannkilder som drikkevann , men også delvis til servicevannformål : nedbørvann , overflatevann i elver , innsjøer , demninger , grunnvann, mineralvann og kildevann . I Tyskland er bruken av vann regulert i vannforvaltningsloven . I Sentral-Europa er det en pålitelig, stort sett kostnadsdekkende og høykvalitets drikkevannsforsyning. Dette er vanligvis garantert av offentlige tilbydere (kommunale leverandører) som tar på seg økologisk ansvar og gjør det tilgjengelig som vann fra springen . Det globale vannmarkedet vokser som ingen annen industri. Det er derfor private leverandører er veldig interessert i å definere vann som en vare for å kunne overta dette markedet.
Der drikkevann ikke er en direkte vare, ble begrepet virtuelt vann introdusert for å ta hensyn til produktets usynlige vanninnhold eller noen ganger høye vannkrav som oppstår i direkte forbindelse med produksjon av et produkt.
Vannforbruk
Mengden vann som forbrukes av mennesker kalles vannforbruk. Det alminnelige uttrykket er - som "energiforbruk" - feil, siden ingen steder er "ødelagt" vann: dets totale mengde på jorden forblir konstant; "Vannbehov" ville være mer passende. Dette inkluderer det umiddelbare konsumet (drikkevann og matlaging ) samt kravene til hverdagen ( vask , skylling av toalett, etc.) samt kravene til landbruk , handel og industri (se industrielt vann ). Dette er derfor ikke bare en parameter for vannmengden som kreves, men for det meste også for deponering eller opparbeiding av avløpsvannet som oppstår ved de fleste vannbruk ( kloakk , renseanlegg ). Mengden av vann som tas fra tilførselsledningen måles ved hjelp av en vannmåleren og benyttet til å beregne kostnadene.
Verdensomspennende ferskvannsbehov er anslått til 4370 km³ (2015), hvor grensen for bærekraftig bruk er angitt til 4000 km³ ( se også World Exhaustion Day ). En faktor som hittil har blitt undervurdert er fordampning av vann som er brukt eller reservert for bruk, for eksempel av planter (" evapotranspirasjon "), som ifølge den nye dataanalysen antas å være rundt 20% av det totale forbruket. [15]
I Tyskland i 1991 var vannbehovet 47,9 milliarder kubikkmeter, hvorav 29 milliarder kubikkmeter ble brukt som kjølevann i kraftverk. Rundt elleve milliarder kubikkmeter ble brukt direkte av industrien, 1,6 milliarder kubikkmeter av landbruket. Bare 6,5 milliarder kubikkmeter ble brukt til å levere drikkevann. Gjennomsnittlig vannbehov (unntatt industri) er rundt 130 liter per innbygger og dag, hvorav rundt 1–2 liter i mat og drikke inkludert vannet i ferdige drikker.
Vanntilgang
Å forsyne mennesket med rent vann utgjør et stort logistisk problem, ikke bare i utviklingsland. Bare 0,3% av verdens vannforsyninger er tilgjengelig som drikkevann, det vil si 3,6 millioner kubikk kilometer av totalt rundt 1,38 milliarder kubikk kilometer.
Vannmangel kan utvikle seg til en vannkrise i land med lite nedbør. Tilpasset teknologi er spesielt egnet for å lindre vannmangel. Imidlertid ble ideer som virket uvanlige også vurdert. Det ble foreslått å dra isfjell over havet til tropiske strøk, som bare ville smelte litt underveis, for å få drikkevann fra dem på destinasjonen.
Se også: vannledningsnettet , vannbehandling , vannbehandlingsanlegg , urban vannforvaltning i Tyskland , vann forurensning
Vanninnhold i noen matvarer
- Smør 18 prosent
- Brød 40 prosent
- Ost 30 til 60 prosent
- Yoghurt, melk 87,5 prosent
- Kjøtt 60-75 prosent
- Eple, pære 85 prosent
- Vannmelon 90 prosent
- Gulrøtter 94 prosent
- Agurker, tomater 98 prosent
Tilgjengelighet av vann
Rundt om i verden har rundt 4 milliarder mennesker eller to tredjedeler av verdens befolkning ikke tilstrekkelig vann tilgjengelig i minst en måned i året. 1,8 til 2,9 milliarder mennesker lider av alvorlig vannmangel i 4 til 6 måneder i året, ca. 0,5 milliarder mennesker hele året. [16] Urbanisering forverrer vannmangel i landlige områder og øker konkurransen mellom byer og landbruk om vann. [17] I tørken og varmen i Europa i 2018 har avlingene i noen tilfeller gått kraftig ned.
Vann som en menneskerett
På forespørsel fra Bolivia erklærte FNs generalforsamling tilgang til rent drikkevann og grunnleggende sanitet for menneskerettigheter 28. juli 2010 med stemmer fra 122 land og uten avvikende stemmer. 41 land avsto, inkludert USA, Canada og 18 EU -land. Siden resolusjoner fra FNs generalforsamling ikke er bindende etter folkeretten, har det i utgangspunktet ingen juridiske konsekvenser. Imidlertid kan den nye resolusjonen nå støtte oppfatningen om at rent vann og sanitet er en del av en "tilstrekkelig" levestandard og derfor kan saksøkes på grunnlag av den internasjonalt bindende internasjonale konvensjonen om økonomiske, sosiale og kulturelle rettigheter , som inneholder rett til tilstrekkelig levestandard . Noen land som Sør -Afrika eller Ecuador har innarbeidet retten til vann i grunnloven. [18]
Gesetzliche Grundlagen und Behörden
Die wasserrechtlichen Grundlagen der Wasserwirtschaft und des öffentlichen Umganges mit den Wasserressourcen bilden in Deutschland das Wasserhaushaltsgesetz und die Europäische Wasserrahmenrichtlinie . Wichtige Behörden und Institutionen sind:
- die Oberen und Unteren Wasserbehörden (auf Kreisebene, je nach Bundesland in Deutschland unterschiedlich)
- Wasser- und Schifffahrtsamt
- LAWA (Arbeitsgemeinschaft)
Wasser in den Wissenschaften
Wasser spielt eine zentrale Rolle in vielen Wissenschaften und Anwendungsgebieten. Die Wissenschaft , die sich mit der räumlichen wie zeitlichen Verteilung des Wassers und dessen Eigenschaften beschäftigt, bezeichnet man als Hydrologie . Insbesondere untersucht die Ozeanologie das Wasser der Weltmeere , die Limnologie das Wasser der Binnengewässer , die Hydrogeologie das Grundwasser und die Aquifere , die Meteorologie den Wasserdampf der Atmosphäre und die Glaziologie das gefrorene Wasser unseres Planeten. In flüssiger Form wurde Wasser bislang nur auf der Erde nachgewiesen. Bereiche der Umweltökonomie befassen sich mit Wasser als Ressource ( Water Economics ).
Wasserchemie
Die Wasserchemie befasst sich mit den Eigenschaften des Wassers, seinen Inhaltsstoffen und mit den Umwandlungen, die im Wasser stattfinden oder durch das Wasser verursacht werden, sowie mit dem Stoffhaushalt der Gewässer. Sie behandelt Reaktionen und Auswirkungen im Zusammenhang mit der Herkunft und Beschaffenheit der unterschiedlichen Wassertypen. Sie beschäftigt sich mit allen Bereichen des Wasserkreislaufs und berücksichtigt damit die Atmosphäre und den Boden. Dabei beschäftigt sie sich unter anderem mit der Analyse von im Wasser gelösten Stoffen, den Eigenschaften des Wassers, dessen Nutzung, dessen Verhaltensweise in verschiedenen Zusammenhängen.
Wasser ist ein Lösungsmittel für viele Stoffe, für Ionenverbindungen, aber auch für hydrophile Gase und hydrophile organische Verbindungen. Sogar gemeinhin als in Wasser unlöslich geltende Verbindungen sind in Spuren im Wasser enthalten. Daher liegt Wasser auf der Erde nirgends in reinem Zustand vor. Es hat je nach Herkunft die unterschiedlichsten Stoffe in mehr oder weniger großen Konzentrationen in sich gelöst.
In der Wasseranalytik unterscheidet man unter anderem folgende Wassertypen:
- Trinkwasser
- Mineralwasser
- Heilwasser
- Tafelwasser
- Süßwasser / Meerwasser / Salzwasser / Brackwasser
- Reinstwasser
- Demineralisiertes Wasser
- Destilliertes Wasser
- Enteisentes Wasser
- Prozesswasser
- Nutzwasser
- Abwasser , (Haushalts-Abwässer, landwirtschaftliche Abwässer, Industrie-Abwässer)
- Regenwasser
- Grundwasser
- Oberflächenwasser (Fließ- und Stehgewässer),
Aber auch bei den wässrigen Auslaugungen (Eluaten) von Sedimenten , Schlämmen, Feststoffen, Abfällen und Böden wird die Wasseranalytik eingesetzt.
Um die Eigenschaften des Wassers und eventuell darin gelöster Stoffe, bzw. damit in Kontakt stehender fester Phasen aufzuklären, kann auch die Molekulardynamik -Simulation sinnvoll sein.
Wasser in den Geowissenschaften
In den Geowissenschaften haben sich Wissenschaften herausgebildet, die sich besonders mit dem Wasser beschäftigen: die Hydrogeologie , die Hydrologie , die Glaziologie , die Limnologie , die Meteorologie und die Ozeanographie . Besonders interessant für die Geowissenschaften ist, wie Wasser das Landschaftsbild verändert (von kleinen Veränderungen über einen großen Zeitraum bis hin zu Katastrophen, bei denen Wasser innerhalb weniger Stunden ganze Landstriche zerstört), dies geschieht zum Beispiel auf folgende Weisen:
- Flüsse oder Meere reißen Erdmassen mit sich und geben sie an anderer Stelle wieder ab ( Erosion ).
- Durch sich bewegende Gletscher werden ganze Landschaften umgestaltet.
- Wasser wird von Steinen gespeichert, gefriert in diesen und sprengt die Steine auseinander, weil es sich beim Gefrieren ausdehnt ( Frostverwitterung ).
- Durch Dürren werden die natürlichen Ökosysteme stark beeinflusst.
Wasser ist nicht nur ein bedeutender Faktor für die mechanische und chemische Erosion von Gesteinen, sondern auch für die klastische und chemische Sedimentation von Gesteinen. Dadurch entstehen unter anderem Grundwasserleiter.
Auch interessiert Geowissenschaftler die Vorhersage des Wetters und besonders von Regenereignissen ( Meteorologie ).
Siehe auch: Gewässer , Permafrostboden , Binnenmeer , Binnensee , Teich , Meer , Ozean , Bach , Flussaue .
Wasser in der Hydrodynamik
Die verschiedenen strömungstechnischen Eigenschaften und Wellentypen in mikroskopischem bis globalem Maßstab werden untersucht, konkret zu folgenden Fragestellungen stehen:
- Optimierung von Bootskörpern und exponierter Baukörper (zum Beispiel Wehre ) – Minimierung des Strömungswiderstandes
- Optimierung des Wirkungsgrades von wassergetriebenen Turbinenrädern und Schiffsantrieben
- Untersuchung von Strömungsphänomenen ( Tsunami , Monsterwellen )
- Wasserstoß ( Wasserwidder )
- Meeresströmungen im Zusammenhang mit Wetter und Klimaerscheinungen
- Strömungen in Gewässern mit Transport und Ablagerung von Sediment , Fischwanderung , Austausch von Sauerstoff, gelösten Stoffen, Plankton
- Hochdruckwasserstrahl als Reinigungs- und Schneidemittel
Wasser und Natur
Vorkommen auf der Erde
Die Bezeichnung Wasser wird im Allgemeinen für den flüssigen Aggregatzustand verwendet. Im festen Zustand spricht man von Eis , im gasförmigen Zustand von Wasserdampf . In der Natur kommt Wasser selten rein vor, sondern enthält meist gelöste Anteile von Salzen, Gasen und organischen Verbindungen.
Verteilung und Verfügbarkeit
Der größte Teil der Erdoberfläche (71 %) ist von Wasser bedeckt, besonders die Südhalbkugel und als Extrem die Wasserhemisphäre . Die Wasservorkommen der Erde belaufen sich auf circa 1,4 Milliarden Kubikkilometer (entspricht dem Volumen eines Würfels mit 1120 km Kantenlänge), wovon der allergrößte Teil auf das Salzwasser der Weltmeere entfällt. Nur 48 Millionen Kubikkilometer (3,5 %) des irdischen Wassers liegen als Süßwasser vor. Das mit 24,4 Millionen Kubikkilometern (1,77 %) meiste Süßwasser ist dabei als Eis an den Polen , Gletschern und Dauerfrostböden gebunden und somit zumindest für prompte Nutzung nicht verfügbar. Einen weiteren wichtigen Anteil macht das Grundwasser mit 23,4 Millionen Kubikkilometern aus. Das Wasser der Fließgewässer und Binnenseen (190.000 km³), der Atmosphäre (13.000 km³), des Bodens (16.500 km³) und der Lebewesen (1.100 km³) ist im Vergleich rein mengenmäßig recht unbedeutend. Dabei ist jedoch nur ein geringer Teil des Süßwassers auch als Trinkwasser verfügbar. Insgesamt liegen 98,233 % des Wassers in flüssiger, 1,766 % in fester und 0,001 % in gasförmiger Form vor. In seinen unterschiedlichen Formen weist das Wasser dabei spezifische Verweilzeiten auf und zirkuliert fortwährend im globalen Wasserkreislauf . Diese Anteile sind jedoch nur näherungsweise bestimmbar und wandelten sich auch stark im Laufe der Klimageschichte , wobei im Zuge der globalen Erwärmung von einem Anstieg des Wasserdampfanteils ausgegangen wird.
Tiefenwasser in schon deutlich wärmeren geologischen Schichten wird direkt oder über Wärmetausch als Wärme-Energiequelle genutzt, wobei sowohl natürliche Thermalquellen und Geysire an der Oberfläche vorliegen als auch der Mensch danach bohrt. Durch den Gebirgsdruck bleibt Wasser in der Tiefe auch bei Temperaturen über dem Siedepunkt bei Normaldruck von 100 °C flüssig. Neue Erkenntnisse lassen vermuten, dass auch in etwa 500 km Tiefe, im Zwischenbereich von oberem und unterem Erdmantel Wasser in flüssiger Form vorliegt. [19]
Die bislang noch fehlende bzw. unzureichende Versorgung eines großen Teils der Weltbevölkerung mit hygienischem und toxikologisch unbedenklichem Trinkwasser , sowie mit einer ausreichenden Menge Nutzwasser , stellt eine der größten Herausforderungen der Menschheit in den nächsten Jahrzehnten dar. Seit 1990 haben rund 2,6 Milliarden weitere Menschen Zugang zu einer sicheren Wasserversorgung erhalten, zum Beispiel mithilfe von Pumpbrunnen oder einem Leitungssystem. Aber immer noch trinken 663 Millionen Menschen jeden Tag Wasser, das verschmutzt ist und krank machen kann. [20]
Herkunft des irdischen Wassers
Die Herkunft des Wassers auf der Erde , insbesondere die Frage, warum auf der Erde deutlich mehr Wasser vorkommt als auf den anderen inneren Planeten, ist bis heute nicht befriedigend geklärt. Ein Teil des Wassers gelangte zweifellos durch das Ausgasen von Magma in die Atmosphäre, stammt also letztlich aus dem Erdinneren . Ob dadurch aber die Menge an Wasser erklärt werden kann, wird stark angezweifelt. Das Element Wasserstoff ist das häufigste Element im Universum, und auch Sauerstoff kommt in großen Mengen vor, allerdings normalerweise gebunden in Silikaten und Metalloxiden; beispielsweise ist der Mars mit großen Anteilen an Eisen(III)-oxid bedeckt, was ihm seine rote Farbe verleiht. Wasser hingegen ist dort – im Vergleich zur Erde – nur in geringen Mengen zu finden.
Vorkommen im Universum
Außerhalb der Erde kommt ebenfalls Wasser vor. Beispielsweise wurde Wassereis in Kometen , auf dem Mars , einigen Monden der äußeren Planeten und dem Exoplaneten OGLE-2005-BLG-390Lb nachgewiesen. Allein die Saturnringe enthalten überschlägig etwa 20 bis 30 Mal so viel Wasser, wie auf der Erde vorkommt. Hinweise auf das Vorhandensein von Wassereis in polnahen Meteoritenkratern gibt es beim Erdmond und sogar beim Merkur , dem sonnennächsten Planeten. Als Flüssigwasser wird es unter den eisigen Oberflächen von Europa , Enceladus , ein paar weiteren Monden sowie bei OGLE-2005-BLG-390Lb vermutet. Direkt fotografisch belegt wurde außerirdisches Flüssigwasser bisher aber nur wenige salzwasserhaltige Schlammtröpfchen auf dem Mars. Außerirdischer Wasserdampf konnte unter anderem in den Atmosphäre von Mars und Titan , den höheren Atmosphärenschichten roter Riesensterne , in interstellaren Nebeln und sogar im Licht ferner Quasare nachgewiesen werden.
Klima
Wasser beeinflusst entscheidend unser Klima und ist Basis nahezu aller Wetter erscheinungen, vor allem bedingt durch seine hohe Mobilität und Wärmekapazität . In den Ozeanen wird die einstrahlende Sonnenenergie gespeichert. Diese regional unterschiedliche Erwärmung führt wegen Verdunstung zu unterschiedlichen Konzentrationen der gelösten Stoffe, da diese nicht mitverdunsten (vor allem Salinität (Salzgehalt)). Dieses Konzentrationsgefälle erzeugt globale Meeresströmungen , die sehr große Energiemengen (Wärme) transportieren (z. B. Golfstrom , Humboldtstrom , äquatorialer Strom , mitsamt ihren Gegenströmungen). Ohne den Golfstrom würde in Mitteleuropa arktisches Klima herrschen.
Im Zusammenhang mit dem Treibhauseffekt stellen Ozeane die wirksamste CO 2 -Senke dar, da Gase wie Kohlendioxid in Wasser gelöst werden ( Kohlenstoffzyklus ). Die mit der globalen Erwärmung einhergehende Temperaturerhöhung der Weltmeere führt zu einem geringeren Haltevermögen an Gasen und damit zu einem Anstieg des CO 2 in der Atmosphäre. Wasserdampf stellt in der Atmosphäre ein wirksames Treibhausgas dar. (siehe Treibhauseffekt )
Bei der Erwärmung verdunstet Wasser, es entsteht Verdunstungskälte . Als „trockener“ Dampf (nicht kondensierend) und als „nasser“ Dampf (kondensierend: Wolken , Nebel ) enthält und transportiert es latente Wärme , die für sämtliche Wetterphänomene entscheidend verantwortlich ist ( siehe auch Luftfeuchtigkeit , Gewitter , Föhn ). Die Wärmekapazität des Wassers und die Phänomene der Verdunstungskälte und latenten Wärme sorgen in der Nähe von großen Gewässern für gemäßigte Klimate mit geringen Temperaturschwankungen im Jahres- und Tagesgang. Wolken verringern zudem die Einstrahlung durch die Sonne und die Erwärmung der Erdoberfläche durch Reflexion .
Der aus Wolken fallende Niederschlag und der Wasserdampf (Auskämmung und Photosynthese bzw. Atmung) bewässern die terrestrischen Ökotope . Auf den Landmassen können so Gewässer oder Eismassen entstehen, die auch meso- und mikroklimatische Wirkungen haben. Das Verhältnis von Evapotranspiration (Gesamtverdunstung eines Gebietes) zu Niederschlag entscheidet, ob sich trockene ( aride , Steppen , Wüsten ) oder feuchte ( humide , Wälder , Waldsteppen ) Klimate bilden. Auf den Landmassen ist außerdem der Wasserhaushalt der Vegetation eine klimatische Größe.
Bedeutung des Wassers für das Leben
Wasser ist vermutlich der Entstehungsort des Lebens und eine seiner Bedingungen. In Organismen und in unbelebten Bestandteilen der Ökosphäre spielt es als vorherrschendes Medium bei fast allen Stoffwechsel vorgängen beziehungsweise geologischen und ökologischen Elementarprozessen eine entscheidende Rolle. Die Erdoberfläche ist zu circa 72 % von Wasser bedeckt, wobei Ozeane hieran den größten Anteil tragen. Süßwasser reserven bilden lediglich 2,53 % des irdischen Wassers und nur 0,3 % sind als Trinkwasser zu erschließen (Dyck 1995). Durch die Rolle des Wassers in Bezug auf Wetter und Klima , als Landschafts gestalter im Zuge der Erosion und durch seine wirtschaftliche Bedeutung, unter anderem in den Bereichen der Land- , Forst- und Energiewirtschaft , ist es zudem in vielfältiger Weise mit Geschichte , Wirtschaft und Kultur der menschlichen Zivilisation verbunden. Die Bedeutung des Wassers für das Leben war insofern auch immer Gegenstand der Naturphilosophie .
Grundbaustein des Lebens
Das Leben ist nach dem heutigen Erkenntnisstand im Wasser entstanden ( siehe auch Evolution ). Autotrophe Schwefelbakterien ( Prokaryoten ) produzieren aus Schwefelwasserstoff und Kohlendioxid unter Zufuhr von Lichtenergie organische Kohlenstoffverbindungen und Wasser:
Als Nachfolger nutzten Blaubakterien ( Cyanobakterien ) und alle späteren autotrophen Eukaryoten das hohe Redoxpotential des Wassers: Unter Zufuhr von Licht produzieren sie aus Wasser und Kohlendioxid Traubenzucker und Sauerstoff:
Durch diesen Prozess reicherte sich im Wasser und in der Atmosphäre immer mehr Sauerstoff an. Damit wurde die Gewinnung von Energie durch Zellatmung ( Dissimilation ) möglich:
Voraussetzung für die Fähigkeit, mit dem giftigen Sauerstoff (Oxidation der empfindlichen Biomoleküle) umzugehen, waren Enzyme wie die Katalase , die eine strukturelle Ähnlichkeit mit dem Sauerstoff transportierenden Hämoglobin aufweist. Aerobe Purpurbakterien nutzten vielleicht als erstes den giftigen Sauerstoff zum energieliefernden Abbau von organischen Stoffen. Nach der Endosymbiontentheorie nahmen damals noch anaerobe Eukaryoten die aeroben Prokaryoten (wahrscheinlich Purpurbakterien) auf.
Wasser wurde damit zum Medium grundlegender biochemischer Vorgänge ( Stoffwechsel ) zur Energiegewinnung und -speicherung:
- Photosynthese , Dissimilation
- Glykolyse
- Zitronensäurezyklus
- Fettabbau
- Eiweißabbau
- Harnstoffzyklus
Auf Grund des Dipolmomentes eignet sich Wasser als Lösungsmittel für polare Substanzen und wegen der daraus entspringenden Viskosität und Dichte als Transportmittel. Wasser transportiert Nährstoffe, Abbauprodukte, Botenstoffe und Wärme innerhalb von Organismen (zum Beispiel Blut , Lymphe , Xylem ) und Zellen. Die Eigenschaften des Wassers werden bei Pflanzen und Tieren (inklusive Mensch) mannigfaltig, z. B. für die Temperaturregulierung benutzt, in Form von Guttation , Schwitzen etc., oder z. B. als Basis für antibakterielle Schutzfilme bei Kröten und Fischen .
Pflanzen und Tieren ohne Skelett verleiht der Turgordruck des Wassers Form und Festigkeit. Durch Turgoränderungen können sie sich auch bewegen (zum Beispiel Blattbewegung bei Pflanzen).
Die Stachelhäuter , zu denen die Seeigel , Seesterne und Seewalzen gehören, haben statt eines festen Skeletts ein System hydraulisch arbeitender Gefäße ( Ambulacralsystem ). Sie bewegen sich durch gezielte Druckänderungen in diesem Gefäßsystem.
Wasser und Ökosysteme
In terrestrischen Ökosystemen ist Wasser begrenzender Faktor der Produktivität. Es ist essenziell für den Stoffwechsel von Lebewesen ( Biosphäre ) sowie für die Herausbildung und Prägung ihrer Standorte ( Pedosphäre , Erdatmosphäre / Klima ). Niederschläge speisen Gewässer und Grundwasser als Ressource für das Pflanzenwachstum und als Trinkwasser für die Tiere.
Die meiste Biomasse und größte Produktivität findet sich in aquatischen Ökosystemen, vor allem in Ozeanen , in denen der begrenzende Produktionsfaktor die Menge der im Wasser gelösten Nährstoffe ist, also vor allem Phosphat, Stickstoffverbindungen (Ammonium, Nitrat) und CO 2 ( Kohlendioxid ). Die Eigenschaften des Wassers werden mit hoher Effizienz genutzt, z. B. bei der Oberflächenspannung von Insekten , Spinnentieren , bei der Dichte und den optischen Eigenschaften vom Plankton etc.
Die Temperaturabhängigkeit der Wasserdichte führt in Gewässern zu einer Temperaturschichtung , zu Sprungschichten und Ausgleichsströmungen, die vor allem in limnischen (Süßwasser-) Biotopen charakteristisch sind ( siehe Ökosystem See ), aber auch in marinen Ökosystemen anzutreffen sind und genutzt werden ( Wale nutzen z. B. die Schallreflexionen an Sprungschichten zur Verbesserung ihrer Kommunikation). Die Dichteanomalie des Wassers ermöglicht auch das Überleben von Lebewesen im Winter, da stehende Gewässer dadurch nicht bis zum Grund durchfrieren (Ausnahme flache Gewässer und „ Frosttrocknis “). Zusätzlich bewirkt die Dichteanomalie in tieferen Seen der gemäßigten Zonen im Frühling und Herbst bei Erreichen einer einheitlichen Temperatur eine Umwälzung des Wassers und somit einen Austausch von Oberflächen- und Tiefenwasser, der für Nährstoff- und Sauerstoffkreislauf wesentlich ist.
Auch wenn aquatische Ökosysteme durch die Wärmekapazität des Wassers sehr stabile Lebensräume darstellen, haben auch geringere Temperaturschwankungen deutliche Folgen (vgl. Ökosystem See ). So wird die Temperaturerhöhung der Ozeane Veränderungen in marinen Ökosystemen zur Folge haben.
Ökologischer Zustand von Gewässern
Der ökologische Zustand von Fließ- bzw. Oberflächengewässern (wie von Grundwasser ) wird in der Europäischen Union (EU) nach der Richtlinie 2000/60/EG (EU-Wasserrahmenrichtlinie, WRRL) nach verschiedenen Kriterien analysiert und nach fünf Graden eingeteilt: „sehr gut“, „gut“, „mäßig“, „unbefriedigend“, „schlecht“. [21] [22]
Wasser in der Technik
Wasser hat in der Technik verschiedene Anwendungsmöglichkeiten, meist im flüssigen Zustand, gelegentlich auch als Eis oder Dampf.
- Die Gewichtskraft von Wassermassen wird in den verschiedenen Wassermühlen und Wasserturbinen zur Gewinnung von mechanischer oder elektrischer Energie genutzt. Beim durch Wasserschlag pumpenden Wasserwidder kommt zusätzlich die geringe Kompressibilität von Wasser dazu.
- Dampf wird genutzt in Dampfturbinen die in vielen modernen Kraftwerken vorkommen um die primär erzeugte Wärme zunächst in mechanische Energie und schließlich mit einem Generator in elektrische Energie umzuwandeln. Die (Kolben-) Dampfmaschine war vor allem in der industriellen Revolution von Bedeutung.
- Eismaschinen dienen der Verarbeitung von Speiseeis und Herstellung von Eiswürfel und Scherbeneis . Die Eisbearbeitungsmaschine zum Glätten der von Kunsteisbahnen . Iglus sind Gebäude aus Eis.
Bei der Wärmeübertragung dient Wasser für Heizung oder in der Wasserkühlung und die Erzeugung von Kälte durch Verdunstung , etwa in Kühltürmen . Den Betrieb von Kältemaschinen auf Basis Adsorption von Ammoniak in Wasser oder Wasserdampf in (wässriger) Lithiumbromid -Lösung.
Wasser dient kalt und warm zum reinigenden Waschen (eventuell mit Detergentien oder Laugen oder Säuren ), Lösen (Auslaugen von Salzlagerstätten), Trennen über Chromatographie oder Extraktion (Aufgussgetränke), Umkristallisieren (Abbinden von Gips, Zement, (zusammen mit Kohlenstoffdioxid:) Kalk; jedoch auch Reinigen von löslichen Substanzen im Chemielabor). Als Druckstrahl zum Spülen, Brausen, Hochdruckreinigen eventuell mit abrasivem Zusatzstoff, und zum Wasserstrahlschneiden auch etwa im hygienesensiblen Bereich der Lebensmittelindustrie.
In Form von Gel als Schallübertragungsmedium vom Sensorkopf zum menschlichen Körper bei der Ultraschalldiagnostik . Wasser ist Schallübertragungsmedium beim Echolot .
Als Medium mit hoher Oberflächenspannung und guter Verdunstungsrate zum verschieblichen Anklatschen von Beschriftungsfolie auf Schaufenstern, Autokarosserien und anderen glatten zu kaschierenden Oberflächen. Auch als Gleit- und Dichtmittel für Saugnäpfe. Die Oberflächenspannung von Wasser erlaubt im Zusammenspiel mit Seife Seifenblasen und das Bauen von Schichten ab Moleküldicke und feiner Membrane für physikalische Experimente. Der Wasserläufer kann mittels Dellen in der Oberfläche laufen, Biofilme können sich ausbreiten, aber auch ölige Substanzen spreiten .
Ursprüngliche Hydraulik verwendet Wasser als Druckübertragungsmedium, als Fontänen in Springbrunnen und Wasserspielen, die auch Verdunstungskühlung und Lichteffekte ermöglichen. Das Aufbrechen von geologischen Schichten beim Fracking ist ebenfalls eine Hochdruckanwendung.
Durch Wasser erzeugter Auftrieb erlaubt Schiffen, Bojen und Lebewesen das Schwimmen. Ballasttanks helfen unbeladene oder ungleichmäßig beladene Schiffe zu stabilisieren und U-Booten auf- und abzutauchen. Es gibt Seilbahnen und Lifte, die im Gegenzug von Wasserballasttanks gezogen bzw. gehoben werden.
Wasser als Dissoziationsmedium dient für Elektrolyse , Galvanik , Akku- und Batterietechnik , in alten Kraftwerken als Strom-Regelungstank. Weiters als Lösungsmittel aller wässrigen Chemie, ob beim Mikroverfahren der Tüpfelplatte , dem grafisch wirksamen Entwickeln fotografischer Platten und Filme oder der großtechnischen Herstellung von Nitramoncal aus Ammoniak und Salpetersäure.
In der Medizin dient Wasser als lösendes Medium zum Injizieren oder Infundieren von Stoffen in den Körper, um den Wasserhaushalt des Körpers zu korrigieren, zum Aufweichen harter Haut oder von Nägeln oder zum Spülen des Darms. Das Kopfhaar mit Wasser reversibel aufzuquellen und in Wellen und Locken zu formen ist Friseurhandwerk .
Weidenruten , Peddigrohr etc. werden in Wasser gelegt zum Flechten biegsam gemacht. Hartholz unter Wasserdampf zu Bugholzmöbeln geformt.
Wasser kann Infrarotstrahlung aus Glühlampenlicht ausfiltern und absorbiert ionisierende Strahlung im Abklingbecken von Kernkraftwerken .
In Wasserwerfern wird Wasser, mit und ohne chemischem Zusatz, als Munition eingesetzt.
Reinstwasser leitet Strom schlecht. Erst, wenn andere Stoffe, die sich in Ionen auflösen können, hinzukommen, kann es elektrischen Strom übertragen. [23]
In Kernkraftwerken wird Wasser als Moderator genutzt, dh, um Neutronen abzubremsen.
Ausstellungen und Veranstaltungen rund ums Wasser
- Von 2005 bis 2014 hat die UNO zur Internationalen Aktionsdekade „Wasser – Quelle des Lebens“ aufgerufen
- Weltwasserforum
- Weltwassertag
- WasserForum – Museum der Wasserversorgung und -gewinnung der HWW ( Hamburger Wasserwerke / Hamburg Wasser )
- Gute Güte – Projekt zur Wasserrahmenrichtlinie der EU in Hannover.
- Wasser (Musical) – Musical von Siegfried Faderl und Ewald Mayrbäurl.
- Wasserleitungsmuseen Kaltenbrunn und Wildalpen der I. Wiener Hochquellenleitung , Wasserspielparks in Wien beim Wasserturm Favoriten und auf der Donauinsel .
Siehe auch
- Brunnen (Heraldik)
- UN-Wasser
- Weltwasserbericht
- Weltwasserrat
Literatur
- Ole Pollem: Regulierungsbehörden für den Wassersektor in Low-Income Countries. Eine vergleichende Untersuchung der Regulierungsbehörden in Ghana, Sambia, Mosambik und Mali . Verlag Dr. Kovac, Hamburg 2009, ISBN 978-3-8300-4473-4 .
Allgemeine Inhalte
- Sibylle Selbmann: Mythos Wasser, Symbolik und Kulturgeschichte. Badenia, Karlsruhe 1995, ISBN 3-7617-0309-0 .
- Philip Ball : H 2 O – Biographie des Wassers. Piper, München 2001, ISBN 3-492-04156-6 .
- Siegfried Dyck , Gerd Peschke: Grundlagen der Hydrologie. 3. Auflage. Verlag für Bauwesen, Berlin 1995, ISBN 3-345-00586-7 .
- Dieter Gerten: Wasser. Knappheit, Klimawandel, Welternährung. CH Beck, München 2018, ISBN 978-3-406-68133-2 .
- Vollrath Hopp: Wasser-Krise? Wasser, Natur, Mensch, Technik und Wirtschaft. Wiley-VCH, Weinheim 2004, ISBN 3-527-31193-9 .
- Ernst Schmidt (Hrsg.): Properties of Water and Steam in SI-Units. Springer, Berlin 1981, ISBN 3-540-09601-9 . („Thermodynamische Eigenschaften von Wasser und Wasserdampf, 0–800 °C, 0–1000 bar“)
- Helmut Lehn, Oliver Parodi: Wasser – elementare und strategische Ressource des 21. Jahrhunderts. I. Eine Bestandsaufnahme. In: Umweltwissenschaften und Schadstoff-Forschung . Band 21, Nr. 3, 2009, S. 272–281.
- Wolfram Mauser: Wie lange reicht die Ressource Wasser? Vom Umgang mit dem blauen Gold . Fischer-Taschenbuch, Frankfurt am Main 2007, ISBN 978-3-596-17273-3 .
- Érik Orsenna : Die Zukunft des Wassers: eine Reise um unsere Welt (Originaltitel: L' avenir de l'eau, übersetzt von Caroline Vollmann). Beck, München 2010, ISBN 978-3-406-59898-2 ; als Taschenbuch: dtv, München 2012, ISBN 978-3-423-34690-0 .
- Helge Bergmann: Wasser Mythen, Märkte, Moleküle. Wiley-VCH, Weinheim 2011, ISBN 978-3-527-32959-5 .
- Leopold Schua: Lebensraum Wasser . Geheimnisse in einer unbekannten Welt. (= Kosmos Bibliothek. Band 268). Stuttgart 1970, ISBN 3-440-00268-3 ( pdf; 23 MB ).
Wasserchemie
- Heinrich Sontheimer, Paul Spindler, Ulrich Rohmann: Wasserchemie für Ingenieure . DVGW-Forschungsstelle am Engler-Bunte-Institut der Uni Karlsruhe. ZfGW-Verlag, Frankfurt 1980, ISBN 3-922671-00-4 .
- Bernd Naumann: Chemische Untersuchungen der Lebensgrundlage Wasser. (= Anregungen zur ökologischen Bildung. Bd. 2). Landesinstitut für Lehrerfortbildung, Lehrerweiterbildung und Unterrichtsforschung von Sachsen-Anhalt (LISA), Halle 1994.
- Günter Wieland: Wasserchemie. 12. Auflage. Vulkan-Verlag, Essen 1999, ISBN 3-8027-2542-5 .
- Karl Höll, Andreas Grohmann ua: Wasser. Nutzung im Kreislauf. Hygiene, Analyse und Bewertung. 8. Auflage. Walter de Gruyter, Berlin 2002, ISBN 3-11-012931-0 . (Standardwerk der Wasseruntersuchung).
- Leonhard A. Hütter: Wasser und Wasseruntersuchung – Methodik, Theorie u. Praxis chemischer, chemisch-physikalischer, biologischer u. bakteriologischer Untersuchungsverfahren. Sauerländer, Frankfurt am Main 1994, ISBN 3-7935-5075-3 .
Nutzung und Schutz
- Christian Opp (Hrsg.): Wasserressourcen. Nutzung und Schutz; Beiträge zum Internationalen Jahr des Süßwassers 2003. Marburger Geographische Gesellschaft, Marburg/Lahn 2004, ISBN 3-88353-049-2 .
- Christian Leibundgut, Franz-Josef Kern: Wasser in Deutschland – Mangel oder Überfluss? In: Geographische Rundschau . Band 58, Nr. 2, 2006, S. 12–19.
Konflikte um Wasser
- Aboubacry Athie: Die politischen Implikationen der Wasserverfügbarkeit in Afrika südlich der Sahara dargestellt am Beispiel der Sahelländer Westafrikas. Wissenschaftlicher Verlag, Berlin 2002, ISBN 3-936846-05-7 .
- Hans Huber Abendroth: Der „Wasserkrieg“ von Cochabamba. Zur Auseinandersetzung um die Privatisierung einer Wasserversorgung in Bolivien. Bundeskammer für Arbeiter und Angestellte, Wien 2004, ISBN 3-7062-0081-3 .
- Detlef Müller-Mahn: Wasserkonflikte im Nahen Osten – eine Machtfrage. In: Geographische Rundschau . Band 58, Nr. 2, 2006, S. 40–48.
- Lisa Stadler, Uwe Hoering: Das Wasser-Monopoly. Von einem Allgemeingut und seiner Privatisierung. Rotpunktverlag, Zürich 2003, ISBN 3-85869-264-6 .
- Karo Katzmann: Schwarzbuch Wasser – Verschwendung, Verschmutzung, bedrohte Zukunft. Molden, Wien 2007, ISBN 978-3-85485-196-7 .
- Andreas Hoppe: Wasser im Nahen Osten – ein Kriegsgrund? In: Naturwissenschaftliche Rundschau . Band 59, Nr. 5, 2006, S. 241–247.
Religiöse Bedeutung
- Claudia Sticher: Wasser. Symbol des Lebens und des Glauben . Mit einem Beitrag von Norbert Lohfink . Verlag Katholisches Bibelwerk, Stuttgart 2014, ISBN 978-3-460-27174-6 .
Lyrisches
Hermann Peter Piwitt und Susann Henschel (Hrsg.): Des Wassers Überfluss – Von Brunnen, Quellen und schönen Wassern , Philipp Reclam jun., Stuttgart 2006, ISBN 978-3-15-018450-9 .
Weblinks
- Wasserlexikon der Uni Bremen
- Grafik, die die weltweite Verteilung von Wasser in allen Formen darstellt
- Sämtliche physikalischen Daten von Wasser (englisch), abgerufen am 25. November 2011
- Das Absorptionsspektrum von flüssigem Wasser vom UV bis zum IR (englisch)
- Grafik, die zeigt, wie es ausshähe, wenn alles Wasser auf oder nahe der Erdoberfläche eine große Kugel bilden würde
- Woher kommt unser Wasser? aus der Fernseh-Sendereihe alpha-Centauri (ca. 15 Minuten). Erstmals ausgestrahlt am 4. Aug. 2002.
- Ist Wasser magisch? aus der Fernseh-Sendereihe alpha-Centauri (ca. 15 Minuten). Erstmals ausgestrahlt am 27. Okt. 2002.
- Marko Pauli: Wasser – Eine rätselhafte Flüssigkeit. In: Deutschlandfunk Kultur – Feature. 16. Januar 2020, abgerufen am 18. Januar 2020 .
- Thema Wasser beim Bundesamt für Umwelt (Schweiz)
Einzelnachweise
- ↑ Das Herkunftswörterbuch (= Der Duden in zwölf Bänden . Band 7 ). 5. Auflage. Dudenverlag, Berlin 2014, S. 915 ( google.de ). Siehe auch DWDS ( „Wasser“ ) und Friedrich Kluge : Etymologisches Wörterbuch der deutschen Sprache . 7. Auflage. Trübner, Straßburg 1910, S. 484 ( digitale-sammlungen.de ).
- ↑ Wasser ist nicht gleich Wasser: Trennung und Untersuchung der Isomere des Wassers (para- und ortho-Wasser, para-Wasser reagiert 25 % schneller mit Diazenylium-Ionen «protonierter Stickstoff»), chemie.de, 31. Mai 2018.
- ↑ Wasser ist nicht gleich Wasser. Universität Basel, 29. Mai 2018.
- ↑ JF Swindells, JR Coe, Jr., and TB Godfrey: Absolute Viscosity of Water at 20 °C . Hrsg.: Journal of Research of the National Bureau of Standards. Band 48 , Nr. 1 , Januar 1952.
- ↑ CE Mortimer, U. Müller: Chemie – Das Basiswissen der Chemie . 12. Auflage. Thieme, 2015, ISBN 978-3-13-484312-5 , S. 61 .
- ↑ Thomas Kramar: Physik: Eine Brücke aus H 2 O . In: Die Presse. 8. November 2007.
- ↑ Wasserstoff als Energieträger der Zukunft ( Memento vom 26. Oktober 2012 im Internet Archive ), VDE, abgerufen am 3. August 2011.
- ↑ Bilden von Strukturen .
- ↑ Sibylle Selbmann: Mythos Wasser. Symbolik und Kulturgeschichte. Badenia Verlag, Karlsruhe 1995, ISBN 3-7617-0309-0 .
- ↑ Hermann Peter Piwitt und Susann Henschel (Hrsg.): Des Wassers Überfluss – Von Brunnen, Quellen und schönen Wassern , Gedichte, Philipp Reclam jun., Stuttgart 2006, ISBN 978-3-15-018450-9 .
- ↑ Deutsche Gesellschaft für Ernährung e. V.: In der Hitze des Sommers viel trinken. Dge.de, 28. Juli 2006, abgerufen am 6. Juli 2010 .
- ↑ Health Marketing – Waterlogged? von Margaret McCartney, doi:10.1136/bmj.d4280 .
- ↑ Linda F. Fried, Paul M. Palevsky: Hyponatremia and Hypernatremia. In: Medical Clinics of North America. Vol. 81, Nr. 3, 1. Mai 1997, S. 585–609. doi:10.1016/S0025-7125(05)70535-6 .
- ↑ Die Wasser-Kältemaschine , BINE Informationsdienst.
- ↑ Dagmar Röhrlich : Ressourcen knapper als gedacht. Deutschlandfunk.de , Forschung Aktuell. 3. Dezember 2015, abgerufen am 3. Dezember 2015. Nach: F. Jaramillo, G. Destouni: Local flow regulation and irrigation raise global human water consumption and footprint . In: Science . Band 350 , Nr. 6265 , 4. Dezember 2015, S. 1248–1251 , doi : 10.1126/science.aad1010 ( sciencemag.org [abgerufen am 29. Mai 2019]).
- ↑ Mesfin M. Mekonnen, Arjen Y. Hoekstra: Four billion people facing severe water scarcity . In: Science . 2016, doi : 10.1126/sciadv.1500323 .
- ↑ Dustin Garrick, Lucia De Stefano ua: Rural water for thirsty cities: a systematic review of water reallocation from rural to urban regions. In: Environmental Research Letters . Band 14, Nr. 4, 2019, S. 043003, doi:10.1088/1748-9326/ab0db7 .
-
↑ Wasser ist ein Menschenrecht. In: Red Globe. 29. Juli 2010, abgerufen am 29. Juli 2010 .
Recht auf Wasser nicht einklagbar. In: der Standard. 29. Juli 2010, abgerufen am 29. Juli 2010 . - ↑ Wolfgang Baumjohann: Dann gehe ich lieber in die Berge. Interview mit Tiz Schaffer. In: Falter . 04/15, 21. Januar 2015. Abgerufen 3. Mai 2015.
- ↑ Zugang zu sauberem Trinkwasser. Abgerufen am 26. Juli 2017 .
- ↑ Umweltziele – der gute Zustand für unsere Gewässer, bmnt.gv.at. Abgerufen am 4. April 2018 .
- ↑ Sibylle Wilke: Ökologischer Zustand der Fließgewässer . In: Umweltbundesamt . 18. Oktober 2013 ( umweltbundesamt.de [abgerufen am 4. April 2018]).
- ↑ Elektrische Leitfähigkeit des Wassers. Abgerufen am 26. April 2021 .
- Wasser
- Wasser (Hydrologie)
- Wasserstoffverbindung
- Sauerstoffverbindung
- Rohstoff